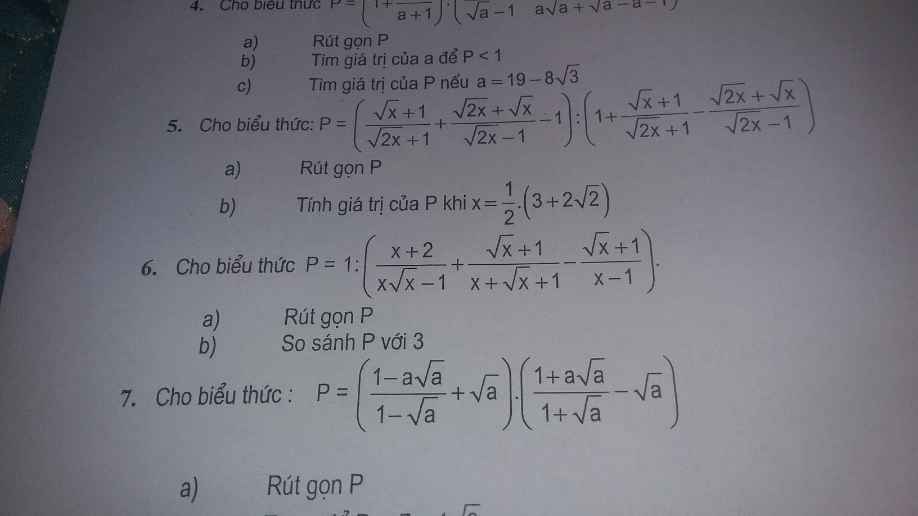
giúp em câu 5,6 với ạ em cảm ơn
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{hh}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH:
CuO + H2 --to--> Cu + H2O
CuO + CO --to--> Cu + CO2
Theo pthh: nCuO = nhh = 0,25 (mol)
=> mCuO = 0,25.80 = 20 (g)

\(=>Qthu1=0,2.340000=68000J\)
\(=>Qthu2=2100.0,2.20=8400J\)
\(=>Qtoa=2.4200.25=210000J\)
\(=>Qthu1+Qthu2< Qtoa\)=>đá nóng chảy hoàn toàn
\(=>0,2.2100.20+0,2.340000+0,2.4200.tcb=2.4200\left(25-tcb\right)\)
\(=>tcb=14,5^oC\)
Cho em hỏi ngu tí ạ vậy tcb ở nhưng phép tính trên vứt đi đâu ạ

a, x x 5,8=19,72
x=19,72:5,8
x=3.4
b,x:5,6=34,5
x=34,5 x 5,6
x=193,2

Bài 5:
\(R_{tđ}=R_1+\dfrac{R_3.R_4}{R_3+R_4}=4+\dfrac{3.6}{3+6}=6\left(\Omega\right)\)
Ta có hiệu điện thế qua vôn kế chính là hiệu điện thế của hai đầu R2,R3
Ta có: \(I_2=\dfrac{U_v}{R_2}=\dfrac{3}{3}=1\left(A\right)\)
\(I_3=\dfrac{U_v}{R_3}=\dfrac{3}{6}=0,5\left(A\right)\)
\(I_1=I_2+I_3=1+0,5=1,5\left(A\right)\)
Hiệu điện thế hai đầu R1 là: \(U_1=R_1.I_1=1,5.4=6\left(V\right)\)
Hiệu điện thế hai đầu AB là: \(U=U_1+U_2=6+3=9\left(V\right)\)
Bài 6:
\(R_{tđ}=R_4+\dfrac{R_2\left(R_1+R_3\right)}{R_2+R_1+R_3}=4,4\left(\Omega\right)\)
\(I_2=\dfrac{U_v}{R_2}=\dfrac{6}{6}=1\left(A\right)\)
\(I_1=I_3=\dfrac{U_v}{R_1+R_3}=\dfrac{6}{3+3}=1\left(A\right)\)
\(I_4=I_2+I_1=1+1=2\left(A\right)\)
Hiệu điện thế hai đầu đoạn mạch AB là: U=I4.Rtđ=2.4,4=8,8(V)

\(n_{Al}=\dfrac{6,48}{27}=0,24\left(mol\right)\)
\(n_{Fe_2O_3}=\dfrac{17,6}{160}=0,11\left(mol\right)\)
PTHH: 2Al + Fe2O3 --to--> Al2O3 + 2Fe
Xét tỉ lệ: \(\dfrac{0,24}{2}>\dfrac{0,11}{1}\) => Hiệu suất tính theo Fe2O3
Gọi số mol Fe2O3 pư là a (mol)
PTHH: 2Al + Fe2O3 --to--> Al2O3 + 2Fe
2a<-----a
=> nAl(sau pư) = 0,24 - 2a (mol)
\(n_{H_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
PTHH: 2KOH + 2Al + 2H2O --> 2KAlO2 + 3H2
0,04<---------------------0,06
=> 0,24 - 2a = 0,04
=> a = 0,1 (mol)
=> \(H\%=\dfrac{0,1}{0,11}.100\%=90,9\%\)
=> B

Câu 7:
a, \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
b, \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT: \(n_{Fe}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,1.56}{10}.100\%=56\%\\\%m_{CuO}=44\%\end{matrix}\right.\)
c, \(n_{CuO}=\dfrac{10-0,1.56}{80}=0,055\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=n_{Fe}+n_{CuO}=0,155\left(mol\right)\)
\(\Rightarrow C\%_{H_2SO_4}=\dfrac{0,155.98}{100}.100\%=15,19\%\)
d, Theo PT: \(\left\{{}\begin{matrix}n_{FeSO_4}=n_{Fe}=0,1\left(mol\right)\\n_{CuSO_4}=n_{CuO}=0,055\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{FeSO_4}=0,1.152=15,2\left(g\right)\\m_{CuSO_4}=0,055.160=8,8\left(g\right)\end{matrix}\right.\)
Câu 8:
a, \(CuCO_3+2HCl\rightarrow CuCl_2+CO_2+H_2O\)
b, \(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo PT: \(n_{CuCO_3}=n_{CO_2}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{CuCO_3}=\dfrac{0,15.124}{20}.100\%=93\%\\\%m_{CuCl_2}=7\%\end{matrix}\right.\)
c, \(n_{HCl}=2n_{CO_2}=0,3\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{0,3}{0,2}=1,5\left(M\right)\)