Dung dịch X chứa Na2SO4 0,3M; MgSO4 0,2M và Fe2(SO4)3 0,1M. Cho dung dịch Ba(NO3)2 từ từ đến dư vào 500 ml dung dịch X thu được m gam kết tủa. Giá trị của m là:
A. 46,6 gam
B. 69,9 gam
C. 93,2 gam
D. 186,4 gam
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H^+}=0,1.2.0,2=0,04\Rightarrow\left[H^+\right]=\dfrac{0,04}{0,2+0,1}\approx0,13M\)
\(n_{SO_4^{2-}}=0,2.0,1+0,3.0,1=0,05\Rightarrow\left[SO_4^{2-}\right]=\dfrac{0,05}{0,2+0,1}\approx0,17M\)
\(n_{Na^+}=0,3.0,1.2=0,06\Rightarrow\left[Na^+\right]=\dfrac{0,06}{0,2+0,1}\approx0,2M\)

Đáp án B
nH+ = 0,05 mol; nOH- = 0,07 mol
H+ + OH- → H2O
Ta thấy H+ hết, OH- dư nên nhúng quỳ tím vào Y thì quỳ tím chuyển thành màu xanh.

a) nNaCl = 1.0,5 = 0,5 (mol) → mNaCl = 0,5.(23 +35,5) = 29,25 (g)
b) nKNO3 = 2.0,5 = 1 (mol) → mKNO3 = 1.101 = 101 (g)
c) nCaCl2 = 0,1.0,25 = 0,025 (mol) → mCaCl2 = 0,025(40 + 71) = 2,775 (g)
d) nNa2SO4 = 0,3.2 = 0,6 (mol) → mNa2SO4 = 0,6.142 = 85,2 (g)

\(n_{H^+}=0.5\cdot\left(0.1+0.3\cdot2\right)=0.35\left(mol\right)\)
\(V_{dd}=a\left(l\right)\)
\(n_{OH^-}=a\cdot\left(0.3+0.2\cdot2\right)=0.7a\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
\(\Rightarrow0.7a=0.35\)
\(\Rightarrow a=0.5\left(l\right)=500\left(ml\right)\)

Định hướng tư duy giải
Ta có:
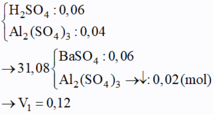
Thêm tiếp Ba(OH)2 kết tủa bị tan 1 phần
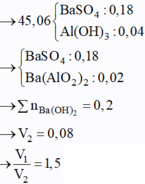

Đáp án A
Hướng dẫn
VX = V; nC6H5OH = 0,2 x 0,2 = 0,04 mol.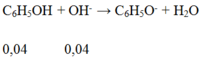
nOH- = 0,2V + 0,3V = 0,04
→ V = 0,08 lít = 80 ml

Đáp án A
VX = V; nC6H5OH = 0,2 x 0,2 = 0,04 mol.
C6H5OH + OH- → C6H5O- + H2O
0,04----------0,04
nOH- = 0,2V + 0,3V = 0,04
→ V = 0,08 lít = 80 ml
Đáp án C
nNa2SO4= 0,15 mol; nMgSO4= 0,1 mol; nFe2(SO4)3=0,05 mol; nSO4(2-)=0,4 mol
Ba2+ + SO42-→ BaSO4
nBaSO4= nSO4(2-)= 0,4 mol; mBaSO4= 93,2 gam