Nung một lượng butan trong bình kín (có xúc tác thích hợp) thu được hỗn hợp khí X gồm ankan và anken. Tỉ khối của X so với khí hidro là 21,75. Phần trăm thể tích của butan trong X là
A. 33,33%
B. 50%
C. 66,67%
D. 25%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : A
Áp dụng công thức: % phản ứng = ![]()
Vậy % thể tích butan = 50%

Đáp án C
MX = 21,75.2 = 43,5. Chọn số mol hỗn hợp X là 1 mol
C4H10 ® CnH2n+2 + CmH2m
a mol a mol a mol
BTKL: ![]()
=> a = 1 – 0,75 = 0,25 mol Þ C4H10 còn dư: 0,75 – 0,25 = 0,5 mol
=> % thể tích C4H10 trong X là 50%

Đáp án C
MX = 21,75.2 = 43,5. Chọn số mol hỗn hợp X là 1 mol
C4H10 → CnH2n+2 + CmH2m
a mol a mol a mol
BTKL: ![]()
=> a = 1 – 0,75 = 0,25 mol
⇒ C4H10 còn dư: 0,75 – 0,25 = 0,5 mol
=> % thể tích C4H10 trong X là 50%

Đáp án C
Giả sử ban đầu có 1 mol C4H10 → m(C4H10) = 58 gam.
BTKL: m(đầu) = m(X) → n(X) = 58 : (23,2.2) = 1,25 mol.
→ n(anken) = n(ankan mới tạo thành) = 1,25 – 1 = 0,25 gam.
→ n(ankan dư) = 1 – 0,25 = 0,75 mol
=> %V(C4H10 trong X) = 0,75 : 1,25 = 60%.

Đáp án C.
![]()
Lấy 1 mol hỗn hớp X. Bảo toàn khối lượng:
![]()
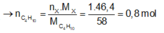
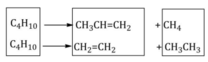
Phản ứng: a mol
Sau phản ứng: b mol
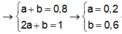
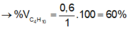

Chọn C.
Giả sử ban đầu có 1 mol C4H10 → m(C4H10) = 58 gam.
BTKL: m(đầu) = m(X) → n(X) = 58 : (23,2.2) = 1,25 mol.
→ n(anken) = n(ankan mới tạo thành) = 1,25 – 1 = 0,25 gam.
→ n(ankan dư) = 1 – 0,25 = 0,75 mol
=> %V(C4H10 trong X) = 0,75 : 1,25 = 60%.
Đáp án B
Chọn 1 mol butan ban đầu. Có: 1C4H10 1 ankan +1 anken
Do đó số mol khí tăng lên chính là số mol C4H10 phản ứng.
Áp dụng định luật bảo toàn khối lượng cho phản ứng ta có: