Hòa tan 1,68 gam kim loại Mg vào V lít dung dịch HNO3 0,25M vừa đủ thu được dung dịch X và 0,448 lít một chất khí Y duy nhất. Cô cạn cẩn thận dung dịch X thu được 11,16 gam muối khan. Công thức phân tử của khí Y và thể tích dung dịch HNO3 đã dùng là:
A. NO và 0,32 lít
B. NO và 0,72 lít
C. N2O và 0,32 lít
D. N2O và 0,72 lít



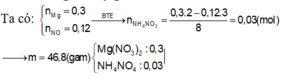
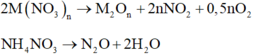
nMg= 0,07 mol=nMg(NO3)2 → mMg(NO3)2= 0,07. 148= 10,36 gam≠ 11,16 gam
→Muối khan phải chứa cả Mg(NO3)2 và NH4NO3
mNH4NO3=11,16- 10,36= 0,8 gam →nNH4NO3= 0,01 mol
Quá trình cho e:
Mg→ Mg2++ 2e (1)
0,07→ 0,14 mol
Quá trình nhận e: nkhí= 0,02mol
NO3-+ 8e + 10H+ → NH4+ + 3H2O (2)
0,08 0,1 0,01 mol
-Nếu khí có 1 nguyên tử N:
N+5 + (5-a) e→ N+a
(5-a).0,02 0,02
Theo ĐL bảo toàn electron có: 0,14= 0,02. (5-a)+0,08→ a= 2 → NO
-Nếu khí có 2 nguyên tử N:
2N+5 + 2(5-a) e→ N2+a
(5-a).0,04 0,02
Theo ĐL bảo toàn electron có: 0,14= 0,04. (5-a) + 0,08→ a= 3,5 loại
Ta có:
NO3-+ 3e+4H+→ NO+ 2H2O (3)
0,06 0,08 0,02 mol
Theo các bán phản ứng (2) và (3)
nH+= 10nNH4++ 4.nNO= 10.0,01+ 4.0,02= 0,18 mol=nHNO3
→V= 0,18/0,25= 0,72 lít
Đáp án B