Một bình chứa 4,8 lít khí hiđrô ở 5 . 10 5 P a ở 14 o C . Người ta tăng nhiệt độ của khí lên tới 26 o C . Vì bình không thật kín nên có một phần khí thoát ra ngoài và áp suất trong bình không thay đổi. Tính khối lượng khí thoát ra ngoài biết khối lượng mol của hiđrô là 2 . 10 - 3 k g / m o l .
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


![]()

Chọn D.
Áp dụng phương trình Cla-pê-rôn – Men-đê-lê-ép:
+ Trạng thái 1 (khi chưa tăng nhiệt độ):
Khối lượng m1, p1 = 5.105 Pa, V1 = 4,8 lít, T1 = 287 K
Từ phương trình:
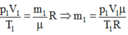
+ Trạng thái 2 (khi đã tăng nhiệt độ):
Khối lượng m2, p2 = p1 = 5.105 Pa, V2 = V1 = 4,8 lít, T2 = 26 + 273 = 287 K.
Từ phương trình:
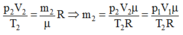
Khối lượng khí thoát ra ngoài:
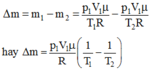
Thay số:
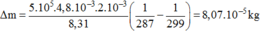

Do bình không dãn nở vì nhiệt, nên công do khí sinh ra : A' = p ∆ V = 0. Theo nguyên lí I, ta có :
∆ U = Q (1)
Nhiệt lượng do khí nhận được : Q = m c V ( T 2 - T 1 ) (2)
Mặt khác, do quá trình là đẳng tích nên :
![]()
Từ (2) tính được : Q = 15,58. 10 3 J.
Từ (1) suy ra: ∆ U = 15,58. 10 3 J.

\(T_1=16^oC=16+273=289K\)
Tăng nhiệt độ khí trong bình lên 1,8 lần thì:
\(T_2=289\cdot1,8=520,2K\)
Áp dụng quá trình đẳng áp:
\(\dfrac{V_1}{T_1}=\dfrac{V_2}{T_2}\)
\(\Rightarrow\dfrac{20}{289}=\dfrac{V_2}{520,2}\)
\(\Rightarrow V_2=36l\)
T1=16oC=16+273=289KT1=16oC=16+273=289K
Tăng nhiệt độ khí trong bình lên 1,8 lần thì:
T2=289⋅1,8=520,2KT2=289⋅1,8=520,2K
Áp dụng quá trình đẳng áp:
V1T1=V2T2V1T1=V2T2
⇒20289=V2520,2⇒20289=V2520,2
⇒V2=36l

Ta có : T1 = toC + 273 = 30 + 273 = 303oK
p1 = 2 bar = 2 . 105 Pa
p2 = 4 bar = 4 . 105
Vì quá trình là đẳng tích , áp dụng định luật Charles ta có
\(\frac{p_1}{p_2}=\frac{T_1}{T_2}\)→ T2 = \(\frac{p_2.T_1}{p_1}=\frac{4.10^5.303}{2.10^5}\)= 606oK
Vậy để áp suất tăng lên gấp đôi , ta phải tăng nhiệt độ lên 606oK
* Trạng thái 1: T1 = 273 + 30 = 303 K
p1 = 2 bar
* Trạng thái 2: T2 = ? p2 = 2p1
* Vì thể tích bình không đổi nên:
\(\frac{P1}{T1}=\frac{P2}{T2}\Rightarrow T2=\frac{P2.T1}{P1}=\frac{2P1.T1}{P1}\) = 2T1 = 606 K

\(\left\{{}\begin{matrix}p_1=10^5Pa\\V_1=80cm^3\\T_1=300^oK\end{matrix}\right.\\ \left\{{}\begin{matrix}p_2=?\\V_2=20cm^3\\T_2=600^oK\end{matrix}\right.\\ \dfrac{p_1V_1}{T_1}=\dfrac{p_2V_2}{T_2}\Leftrightarrow\dfrac{10^5.80}{300}=\dfrac{p_2.20}{600}\\ \Rightarrow p_2=8.10^5Pa\)

T1 = 27 + 273 = 300K
T2 = 327 + 273 = 600K
Phương trình trạng thái khí lí tưởng:
\(\dfrac{P_1V_1}{T_1}=\dfrac{P_2V_2}{T_2}\Rightarrow\dfrac{10^5.120}{300}=\dfrac{P_2.20}{600}\Leftrightarrow\dfrac{12000000}{300}=\dfrac{20P_2}{600}\)
=> 20P2 = 24000000
=> P2 = 1200000Pa
phương trình trạng thái lí tưởng:
\(\dfrac{P_1.V_1}{T_1}=\dfrac{P_2.V_2}{T2}\)
Theo đề bài:
V1 = 120cm3; T1 = 27 + 273 = 300K ; P1 = \(10^5\)Pa
V2 = 20cm3; T2 = 327 + 273 = 600K
Thay vào phương trình:
\(\dfrac{10^5.120}{300}=\dfrac{P_2.20}{600}\Rightarrow P_2=\dfrac{P_1.T_2.V_2}{V_2.T_1}=1200000Pa\)
=12.10^5 Pa

Đáp án: B
Vì thể tích của bóng đèn không đổi nên ta có:
p 1 T 1 = p 2 T 2 → p 2 = T 2 T 1 p 1 = 40 + 273 20 + 273 .1,5.10 5 = 1,6.10 5 (pa)