Cho 2,24 gam hỗn hợp G gồm: CaCO3 và Mg vào một lượng vừa đủ m gam dd HCl 10%. Sau phản ứng thu được dd A và 0,672 lít hỗn hợp khí B ở đktc. Xác định % khối lượng của các chất trong G và khối lượng dung dịch HCl đã dùng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

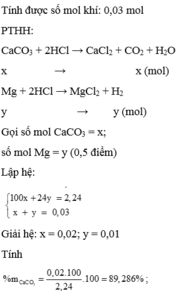
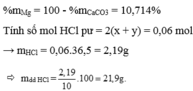

\(n_{H2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,03 0,06 0,03 0,03
\(MgO+2HCl\rightarrow MgCl_2+H_2O|\)
1 2 1 1
0,03 0,06 0,03
a) \(n_{Mg}=\dfrac{0,03.1}{1}=0,03\left(mol\right)\)
\(m_{Mg}=0,03.24=0,72\left(g\right)\)
\(m_{MgO}=1,92-0,72=1,2\left(g\right)\)
b) Có : \(m_{MgO}=1,2\left(g\right)\)
\(n_{MgO}=\dfrac{1,12}{40}=0,03\left(mol\right)\)
\(n_{HCl\left(tổng\right)}=0,06+0,06=0,12\left(mol\right)\)
400ml = 0,4l
\(C_{M_{ddHCl}}=\dfrac{0,12}{0,4}=0,3\left(l\right)\)
c) \(n_{MgCl2\left(tổng\right)}=0,03+0,03=0,06\left(mol\right)\)
\(C_{M_{MgCl2}}=\dfrac{0,06}{0,4}=0,15\left(M\right)\)
Chúc bạn học tốt

\(n_{CO2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH : \(CaO+2HCl\rightarrow CaCl_2+H_2O\) (1)
\(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\) (2)
a) Theo Pt : \(n_{CO2}=n_{CaCO3}=0,1\left(mol\right)\)
\(m_{CaCO3}=0,1100=10\left(g\right)\)
\(m_{CaO}=12,8-10=2,8\left(g\right)\)
b) Chắc tính V của dd HCl đã dùng
(1) \(n_{CaO}=\dfrac{2,8}{56}=0,05\left(mol\right)\) , \(n_{HCl}=2n_{CaO}=0,1\left(mol\right)\)
(2) \(n_{HCl}=2n_{CaCO3}=0,2\left(mol\right)\)
\(\Rightarrow V_{ddHCl}=\dfrac{0,1+0,2}{1}=0,3\left(l\right)=300\left(ml\right)\)

a)
\(Zn + 2HCl \to ZnCl_2 + H_2\\ Fe_2O_3 + 6HCl \to 2FeCl_3 + 3H_2\)
Theo PTHH : \(n_{Zn} = n_{H_2} = \dfrac{6,72}{22,4} = 0,3(mol)\)
\(\Rightarrow n_{Fe_2O_3} = \dfrac{35,5-0,3.65}{160} = 0,1\\ \Rightarrow n_{HCl} = 2n_{Zn} + 6n_{Fe_2O_3} = 0,3.2 + 0,1.6 = 1,2(mol)\\ \Rightarrow m_{HCl} = 1,2.36,5 = 43,8(gam)\)
b)
\(CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O\)
Gọi \(n_{CuO} = a;n_{Fe_2O_3} = b\)
\(\left\{{}\begin{matrix}80a+160b=19,6\\a+3b=0,3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,135\\b=0,055\end{matrix}\right.\)
Vậy :
\(\left\{{}\begin{matrix}n_{Cu}=0,135\\n_{Fe}=0,055.2=0,11\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}m_{Cu}=0,135.64=8,64\left(gam\right)\\m_{Fe}=0,11.56=6,16\left(gam\right)\end{matrix}\right.\)

Câu 5 :
\(n_{H2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
a) Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,1 0,2 0,1 0,1
\(MgO+2HCl\rightarrow MgCl_2+H_2O|\)
1 2 1 1
0,15 0,3 0,15
a) \(n_{Mg}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(m_{Mg}=0,1.24=2,4\left(g\right)\)
\(m_{MgO}=8,4-2,4=6\left(g\right)\)
0/0Mg = \(\dfrac{2,4.100}{8,4}=28,57\)0/0
0/0MgO = \(\dfrac{6.100}{8,4}=71,43\)0/0
b) Có : \(m_{MgO}=6\left(g\right)\)
\(n_{MgO}=\dfrac{6}{40}=0,15\left(mol\right)\)
\(n_{HCl\left(tổng\right)}=0,2+0,3=0,5\left(mol\right)\)
\(m_{HCl}=0,5.36,5=18,25\left(g\right)\)
\(m_{ddHCl}=\dfrac{18,25.100}{3,65}=500\left(g\right)\)
\(n_{MgCl2\left(tổng\right)}=0,1+0,15=0,25\left(mol\right)\)
⇒ \(m_{MgCl2}=0,15.95=14,25\left(g\right)\)
\(m_{ddspu}=8,4+500-\left(0,1.2\right)=508,2\left(g\right)\)
\(C_{MgCl2}=\dfrac{14,25.100}{508,2}=2,8\)0/0
Chúc bạn học tốt




