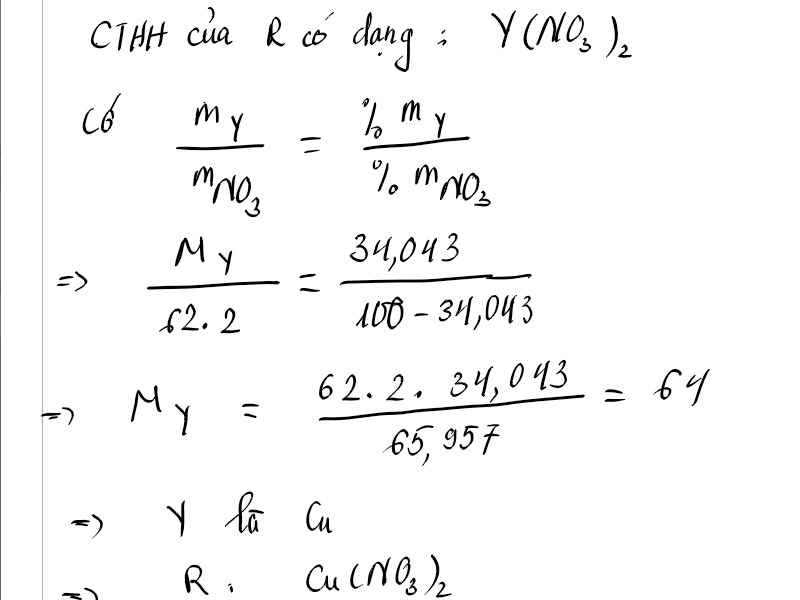Giúp em với ạ.
Hợp chất A có phân tử khối 175< A < 185 được tạo bởi kim loại R có hóa trị II và nhóm ngyên tử XOy có htri I. Biết rằng phần trăm của X trong hợp chất A là 15,556% và Y không lớn hơn 3. Xác định tên nguyên tố R.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Hợp chất X : $R_2O_5$(lập CTHH dựa quy tắc hóa trị)
$M_X = 2R + 5O = 2R + 16.5 = 142\ đvC \Rightarrow R = 31(đvC)$
Vậy R là nguyên tố Photpho, CTHH X : $P_2O_5$
Hợp chất Y : $A_2(SO_4)_a$(lập CTHH dưa quy tắc hóa trị )
$M_Y = 2A + 96a =142 : 0,355 = 400\ đvC$
Với a = 1 thì A = 152 - loại
Với a = 2 thì A = 104 - loại
Với a = 3 thì A = 56 (Fe)
Vậy A là nguyên tố Fe, CTHH Y : $Fe_2(SO_4)_3$

áp dụng quy tắc hóa trị thì công thức hóa học đơn giản là
R2(SO4)3
theo đề bài ta có
PTK[R2(SO4)3]=400(dvC)
=>PTK(R2)=400-(32+16*4)*3=112(dvC)
=>NTK(R)=112:2=56(dvC)
=> R là sắt (Fe)
Đặt CTPT của chất là Rx(SO4)y (x, y nguyên dương)
Theo quy tắc hóa trị, ta có: x.III = y.II
=> \(\dfrac{x}{y}=\dfrac{2}{3}\)
=> CTHH của chất lả R2(SO4)3
=> 2.R + (32 + 16.4).3 = 400
=> R = 56 (đvC)

\(CTHH:ASO_4\\ PTK_{ASO_4}=NTK_A+NTK_S+4NTK_O=5PTK_{O_2}\\ \Rightarrow NTK_A+32+64=160\\ \Rightarrow NTK_A=64\left(đvC\right)\\ \Rightarrow A\text{ là đồng }\left(Cu\right)\)

Nguyên tử X (chỉ có 1 hóa trị trong hợp chất) tạo với oxi hợp chất có công thức X2O3. Phân tử hợp chất tạo bởi X và nhóm NO3 (I) có phân tử khối bằng 213đvC. Xác định nguyên tử khối của X. Viết công thức hợp chất của X với oxi, X với nhóm NO3.
Ta có Nguyên tử X (chỉ có 1 hóa trị trong hợp chất) tạo với oxi hợp chất có công thức X2O3.
=>X hóa trị 3
=> công thức với NO3 là
X(NO3)3
phân tử khối bằng 213đvC.
=>X+14.3+16.3.3=213
=>X=27 (nhôm )Al
=> công thức là Al2O3, Al(NO3)3

Đ
ặ
t
:
Y
(
N
O
3
)
2
V
ì
:
%
m
Y
=
34
,
043
%
⇔
M
Y
M
Y
+
124
=
34
,
043
%
⇔
M
Y
=
64
(
g
m
o
l
)
⇒
Y
:
Đ
ồ
n
g
(
C
u
=
64
)
⇒
C
T
H
H
:
C
u
(
N
O
3
)
2
Thu gọn