Cần ít nhất bao nhiêu ml dung dịch HCl 1M cần cho vào 500 ml dung dịch Na Al OH 4 0,1M để thu được 0,78 g chất kết tủa?
A. 10 ml
B. 100 ml
C. 15 ml
D. 170 ml
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
• V lít HCl 1M + 0,05 mol Na[Al(OH)4] → 0,01 mol ↓Al(OH)3
Cần ít nhất HCl → HCl thiếu
HCl + Na[Al(OH)4] → NaCl + Al(OH)3↓ + H2O
nHCl = 0,01 mol → VHCl = 0,01 : 1 = 0,01 lít = 10 ml

Đáp án: B.
3 N a 2 C O 3 + A l 2 ( S O 4 ) 3 + 3 H 2 O → 2 A l ( O H ) 3 ↓ + 3 C O 2 + 3 N a 2 C O 4
3 mol 1 mol
x mol 0,025 x 0,02 mol
⇒ x = 0,0015 mol
![]()

Câu 2 :
$n_{HCl} = 0,2.1 + 0,3.1,5 = 0,65(mol)$
$V_{dd} = 0,2 + 0,3 = 0,5(mol)$
$C_{M_{HCl}} = \dfrac{0,65}{0,5} =1,3M$
Câu 3 :
Gọi $m_{H_2O\ cần\ thêm} =a (gam)$
Sau khi thêm :
$m_{NaOH} = 100.35\% = 35(gam)$
$m_{dd} = 100 + a(gam)$
Suy ra: $\dfrac{35}{100 + a}.100\% = 20\%$
Suy ra: a = 75(gam)
Câu 4 :
Gọi $V_{dd\ HCl\ 2M} =a (lít) ; V_{dd\ HCl\ 3M} = b(lít)$
Ta có :
$a + b = 4$
$2a + 3b = 4.2,75$
Suy ra a = 1(lít) ; b = 3(lít)

Chọn A
Để đạt V lớn nhất thì sẽ xảy ra trường hợp tạo kết tủa sau đó kết tủa tan 1 phần.
OH- + H+ → H2O
[Al(OH)4]- + H+ → Al(OH)3 ↓ + H2O Al(OH)3 + 3H+ → Al3+ + 3H2O
nH+ = nOH- + 4nAlO2- - 3nAl(OH)3 = 0,3.0,6 + 4.0,3.1- 3. = 0,78 mol
→ VHCl = 390 ml

Đáp án B
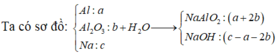
Khi cho 0,06 mol HCl ⇒ m gam kết tủa. Thêm tiếp vào (0,13–0,06) = 0,07 mol thì số mol kết tủa giảm 0,01 mol.
⇒ Khi cho 0,06 mol HCl vào thì kết tủa chưa đạt cực đại. Với 0,13 mol HCl thì số mol kết tủa đã đạt cực đại và bị hòa tan lại.
⇒ Sau khi phản ứng với 0,06 mol HCl thì số mol NaAlO2 còn lại = 0 , 07 - 0 , 01 × 3 4 = 0 , 01 m o l
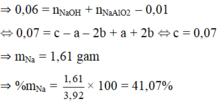
Đáp án cần chọn là: A