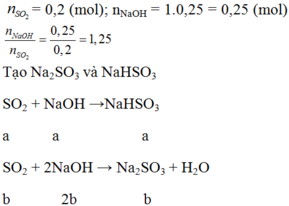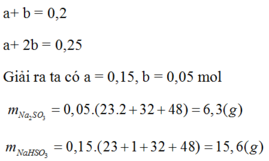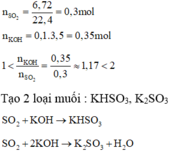Hấp thụ hoàn toàn 8,96 lít khí SO2 (đktc) vào 500ml dung dịch NaOH 1,2M. Tính khối lượng muối tạo thành sau phản ứng, tính nồng độ mol của muối sau phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{SO_2}=\dfrac{8.96}{22.4}=0.4mol\)
\(n_{NaOH}=0.5mol\)
Lập tỉ lệ: \(\dfrac{n_{NaOH}}{n_{SO_2}}=\dfrac{0.5}{0.4}=1.25\)
=> Thu được 2 muối \(NaHSO_3\) và \(Na_2SO_3\)
\(SO_2+NaOH\rightarrow NaHSO_3\)
a a a
\(SO_2+2NaOH\rightarrow Na_2SO_3+H_2O\)
b 2b b
Ta có: \(\left\{{}\begin{matrix}a+b=0.4\\a+2b=0.5\end{matrix}\right.\)\(\Leftrightarrow\left\{{}\begin{matrix}a=0.3\\b=0.1\end{matrix}\right.\)
Khối lượng muối thu được: \(m_{muoi}=0.3\times104+0.1\times126=43.8g\)


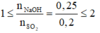 ⇒ phản ứng tạo 2 muối
⇒ phản ứng tạo 2 muối
Phương trình hóa học của phản ứng
SO2 + NaOH → NaHSO3
SO2 + 2NaOH → Na2SO3 + H2O
Gọi nNa2SO3 = x mol; nNaHSO3 = y mol
nNaOH = 2x + y = 0,25.
nSO2 = x + y = 0,2.
Giải ra ta có: x = 0,05, y = 0,15.
mNaHSO3 = 0,15 x 104 = 15,6g.
mNa2SO3 = 0,05 x 126 = 6,3g.

Ta thấy khi cho Br 2 vào dung dịch 2 muối S 4 + thì toàn bộ S 4 + sẽ bị oxi hoá lên S 6 + ( SO 4 2 - )do đó :
n SO 2 = n SO 4 2 - = 0,15
=> m BaSO 4 = 0,15.233 = 34,95g

Bài 32:
a, \(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=0,5.0,2=0,1\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{n_{CO_2}}{n_{Ca\left(OH\right)_2}}=\dfrac{0,15}{0,1}=1,5\) → Pư tạo 2 muối: CaCO3 và Ca(HCO3)2.
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
\(2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2\)
Gọi: \(\left\{{}\begin{matrix}n_{CaCO_3}=x\left(mol\right)\\n_{Ca\left(HCO_3\right)_2}=y\left(mol\right)\end{matrix}\right.\)
Theo PT: \(\left\{{}\begin{matrix}n_{CO_2}=n_{CaCO_3}+2n_{Ca\left(HCO_3\right)_2}=x+2y=0,15\\n_{Ca\left(OH\right)_2}=n_{CaCO_3}+n_{Ca\left(HCO_3\right)_2}=x+y=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,05\left(mol\right)\\y=0,05\left(mol\right)\end{matrix}\right.\) \(\Rightarrow m_{CaCO_3}=0,05.100=5\left(g\right)\)
b, mCO2 = 0,15.44 = 6,6 (g) > mCaCO3 → m dd tăng.
Bài 33:
a, \(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=0,6.0,5=0,3\left(mol\right)\)
Ta có: \(\dfrac{n_{CO_2}}{n_{Ca\left(OH\right)_2}}=\dfrac{0,4}{0,3}=1,33\) → Pư tạo muối: CaCO3 và Ca(HCO3)2.
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
\(2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2\)
Gọi: \(\left\{{}\begin{matrix}n_{CaCO_3}=x\left(mol\right)\\n_{Ca\left(HCO_3\right)_2}=y\left(mol\right)\end{matrix}\right.\)
Theo PT: \(\left\{{}\begin{matrix}n_{CO_2}=n_{CaCO_3}+2n_{Ca\left(HCO_3\right)_2}=x+2y=0,4\\n_{Ca\left(OH\right)_2}=n_{CaCO_3}+n_{Ca\left(HCO_3\right)_2}=x+y=0,3\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\) \(\Rightarrow m_{CaCO_3}=0,2.100=20\left(g\right)\)
b, mCO2 = 0,4.44 = 17,6 (g) < mCaCO3 → m dd giảm.