1) Nêu hiện tượng và viết phản ứng xảy ra (nếu có) trong các thí nghiệm sau:
a) Dẫn khí SO2 vào dung dịch nước brom loãng(có màu vàng nâu)
b) Dẫn khí H2S vào dung dịch Pb(NO3)2
c) Mở nắp lọ đựng dung dịch H2S sau 1 thời gian
d) Nhỏ dung dịch H2SO4 vào ống đựng dung dịch Ba(NO3)2
2) Viết phương trình chứng minh:
a) Khí sunfuro có tính oxi hóa
b) H2S có tính khử mạnh
c) Axit sunfuric đặc có tính oxi hóa mạnh
d) Ozon có tính oxi hóa mạnh hơn oxi
e) S có tính khử

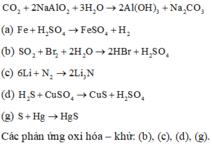
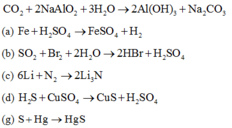
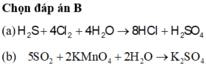
Câu 1:
a, Hiện tượng: dung dịch Brom nhạt màu dần
- PTHH: SO2 + Br2 + 2H2O → H2SO4 + 2HBr
b, Hiện tượng: Xuất hiện kết tủa màu đen
- PTHH: H2S + Pb(NO3)2 → PbS + 2HNO3
c, Hiện tượng : Bị vẫn đục màu vàng
- PTHH: 2H2S + O2 → S + 2H2O
d, Hiện tượng: Xuất hiện kết tủa trắng
PTHH: H2SO4 + Ba(NO3)2 → BaSO4 + 2HNO3
Câu 2:
a) SO2 + 2H2S \(\underrightarrow{^{t^o}}\)3S + 2H2O
b) H2S + 2FeCl3 → 2FeCl2 + S + 2HCl
c) Cu + 2H2SO4 đặc → CuSO4 + SO2 + 2H2O
d) O3 +2 Ag → Ag2O + O2
e) S + O2 \(\underrightarrow{^{t^o}}\) SO2
to nhé