cho 4,64 gam hỗn hợp chứa FeO,Fe3O4,F2O3 trong đó số mol FeO bằng số mol Fe2O3 tác dụng vừa đủ với dung dihcj HCl 1M thu được dung dịch X.
a) tính thể tích dung dịch HCl cần dùng cho phản ứng trên
b) cố cạn dung dịch X thu được m gam muối khan . tính m



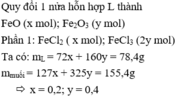

Vì số mol FeO bằng Fe2O3.
\(FeO+Fe_2O_3\rightarrow Fe_3O_4\)
Quy đổi hỗn hợp chỉ gồm Fe3O4.
\(Fe_3O_4+8HCl\rightarrow FeCl_2+2FeCl_3+4H_2O\)
\(\Rightarrow n_{Fe3O4}=\frac{4,64}{56.3+16.4}=0,02\left(mol\right)\)
\(\Rightarrow n_{HCl}=8n_{Fe3O4}=0,16\left(mol\right)\)
\(\Rightarrow V_{HCl}=\frac{0,16}{1}=0,16\left(l\right)\)
Theo phản ứng: \(n_{H2O}=\frac{1}{2}n_{HCl}=0,08\left(mol\right)\)
BTKL:
\(m_{Fe3O4}+m_{HCl}=m_{muoi}+m_{H2O}\)
\(=4,64+0,16.36,5=m_{muoi}+0,08.18\)
\(\Rightarrow m_{muoi}=9,04\left(g\right)\)