Đốt cháy hết m (gam) một mẫu than (chứa 4% tạp chất trơ, còn lại là cacbon) bởi V(lít) khí Oxi thu được 2,24 lít hỗn hợp chất khí x (dktc). Sục khí X vào dung dịch nước vôi trong dư thấy tạo thành 8 gam kết tủa. Tính giá trị của m và V biết thể tích các khí đều do ở dktc

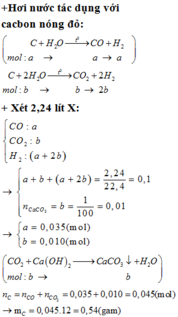

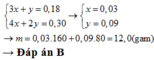



X gồm O2 dư và CO2
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
\(n_{CaCO3}=n_{CO2}=0,08\left(mol\right)\)
\(n_X=0,1\left(mol\right)\)
\(\Rightarrow n_{O2_{Dư}}=0,02\left(mol\right)\)
\(C+O_2\underrightarrow{^{to}}CO_2\)
\(\Rightarrow n_C=n_{O2_{pu}}=n_{CO2}=0,08\left(mol\right)\)
Tổng nO2= 0,08 + 0,02 = 0,1 mol
\(\Rightarrow V=0,1.22,4=2,24\left(l\right)\)
\(m_C=0,08.12=0,96\left(g\right)\)
Than chứa 96% C nên lượng than đem đốt là 0,96:96%= 1g
Sao biết đc trong X gồm O2 dư và CO2 đc ạ?
Cần thông não