Hòa tan 8,2 gam hỗn hợp bột CaCO3 và MgCO3 trong nước cần 2,016 lít CO2 (đktc). Xác định số gam mỗi muối trong hỗn hợp.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi x, y lần lượt là số mol CaCO3 và MgCO3 trong hỗn hợp
Số mol CO2 là:
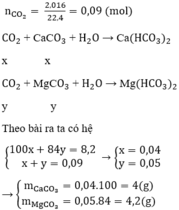

CaCO3 + H2SO4 --> CaSO4 + CO2 + H2O
x x x
MgCO3 + H2SO4 --> MgSO4 + CO2 + H2O
y y y
nCO2=\(\dfrac{0,896}{22,4}\)=0,04
100x+84y=3,68
x+y=0,04
\(\left\{{}\begin{matrix}x=0,02\\y=0,02\end{matrix}\right.\)
%mCaCO3=\(\dfrac{0,02.100}{3,68}\)=54,35%
%mMgCO3=100-54,35=45,65%
mCaSO4=0,02.136=2,72g
mMgSO4=0,02.120=2,4g

cÂU 2.
\(n_Z=\dfrac{6,72}{22,4}=0,3mol\)
\(\left\{{}\begin{matrix}n_{CaCO_3}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\Rightarrow100x+56y=25,6\left(1\right)\)
\(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(\Rightarrow x+y=n_Z=0,3\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
\(\%m_{CaCO_3}=\dfrac{0,2\cdot100}{25,6}\cdot100\%=78,125\%\)
\(\%m_{Fe}=100\%-78,125\%=21,875\%\)
\(m_{muối}=m_{CaCl_2}+m_{FeCl_2}=0,2\cdot111+0,1\cdot127=34,9g\)

Gọi số mol của CaCO3 và MgCO3 trong hỗn hợp là x, y.
CaCO3 + CO2 + H2O → Ca(HCO3)2
x x (mol)
MgCO3 + CO2 + H2O → Mg(HCO3)2
y y (mol)
Ta có hệ phương trình: => x = 0,04; y 0,05
=>m CaCO3 = 0,04.100 = 4 (gam)
mMgCO3 = 84.0,05 = 4,2 (gam)

Ta có: \(n_{CO_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
a. PTHH:
\(MgCO_3+H_2SO_4--->MgSO_4+H_2O+CO_2\)
\(MgSO_4+H_2SO_4--\times-->\)
b. Theo PT: \(n_{MgCO_3}=n_{CO_2}=0,03\left(mol\right)\)
\(\Rightarrow m_{MgCO_3}=0,03.84=2,52\left(g\right)\)
\(\Rightarrow m_{MgSO_4}=6-2,52=3,48\left(g\right)\)
\(\Rightarrow\%_{m_{MgCO_3}}=\dfrac{2,52}{6}.100\%=42\%\)
\(\%_{m_{MgSO_4}}=100\%-42\%=58\%\)
c. Theo PT: \(n_{MgSO_4}=n_{CO_2}=0,03\left(mol\right)\)
\(\Rightarrow m_{MgSO_4}=0,03.120=3,6\left(g\right)\)
\(\Rightarrow m_{MgSO_{4_{thu.được.sau.phản.ứng}}}=3,6+3,48=7,08\left(g\right)\)
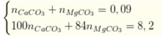
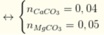
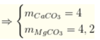
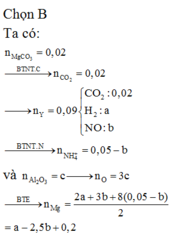
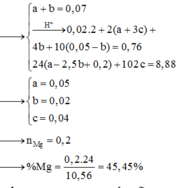


Gọi x, y lần lượt là số mol CaCO3 và MgCO3 trong hỗn hợp
Số mol CO2 là: