Trộn 100ml dung dịch Fe2(SO4)3 với 100ml dung dịch Ba(OH)2 sau phản ứng thu được kết tủa A và dung dịch B. Nung A ở nhiệt độ cao đến khối lượng không đổi thu được 4,295 gam chất rắn D. Khi cho dung dịch B tác dụng vừa đủ với 100ml dung dịch H2SO4 thì thu được 0,932gam kết tủa.
a) Viết phương trình phản ứng xảy ra
b) Xác định Cm của dung dịch Fe2(SO4)3 và Ba(OH)2 ban đầu.



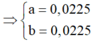
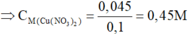
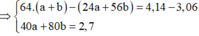
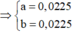

Fe2(SO4)3+3Ba(OH)2\(\rightarrow\)2Fe(OH)3+3BaSO4
2Fe(OH)3\(\rightarrow\)Fe2O3+3H2O
Ba(OH)2+H2SO4\(\rightarrow\)BaSO4+2H2O
Ta có
ddB+H2SO4 tạo kết tủa \(\rightarrow\)dd B là Ba(OH)2 dư
Kết tủa A gồm Fe(OH)3 và BaSO4
Chất rắn D gồm Fe2O3 và BaSO4
nBaSO4=\(\frac{0,932}{233}\)=0,004 mol
\(\rightarrow\)nBa(OH)2 dư=0,04 mol
Gọi a là số mol Fe2(SO4)3\(\rightarrow\)nBa(OH)2 tham gia=3a mol
nBaSO4=3a mol
nFe2O3=a mol
Ta có
160a+699a=4,295 \(\rightarrow\)a=0,005 mol
\(\rightarrow\) nFe2(SO4)3=0,005 mol
nBa(OH)2=0,005.3+0,004=0,019 mol
CMFe2(SO4)3=\(\frac{0,005}{0,1}\)=0,05 M
CMBa(OH)2=\(\frac{0,019}{0,1}\)=0,19 M