Hòa tan 5,4 Al vào dung dịch H2 SO4 , vào PƯ thu được Al2(SO4)3;4,48l khí H2 và 1 chất rắn X. Đốt cháy X ở t° cao thu được chất rắn Y.
a. Thính khối lượng của H2SO4 cần dùng.
b. Tính mY và Vo2 cần dùng?
Giúp mình với, mình đang cần bài này rất gấp ヾ(❀╹◡╹)ノ゙❀~ cảm ơn rất nhiều a~



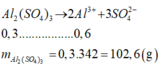
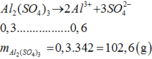
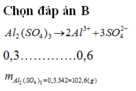
a,nAl=0,2 mol
nH2=0,2 mol
PTPU: 2Al+3h2so4-->al2(so4)3+3H2
viết pt rồi sau đó điền số mol al và h2 vào phương trình
ta có: 0,2/2>0,2/3
-->Al dư--> tính theo H2
Viết lại phương trình :2Al+3h2so4-->al2(so4)3+3H2
Điển số mol h2, điền số mol h2so4
nH2SO4=nH2=0,2 mol --> khối lg h2so4 cần dùng là : 0,2.98=19,6 b,Số mol al dư là : 0,2-0,2/3.2=1/15 mol PTPU: 2al+3o2-->2al2o3 điền số mol al dư vào pt, tính đc số mol o2 và al2o3 Còn lại tương tự nhé