a) Cho 7,2 gam một kim loại M có hóa trị II tác dụng hết với axit clohiđric thì thu được 6,72 lít khí H2 (ở đktc). Xác định kim loại M.
b) Cho 10,8 gam một kim loại M có hóa trị không đổi tác dụng với dung dịch sunfuric loãng dư thu được 13,44 lít khí H2 (đktc). Xác định kim loại M?

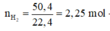
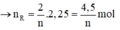
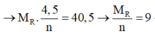
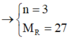
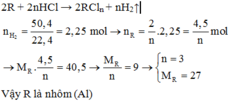
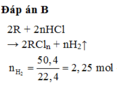
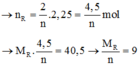
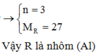

a) PTHH: M + 2HCl \(\rightarrow\) MCl2 + H2\(\uparrow\)
n\(H_2\) = \(\frac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: nM = n\(H_2\) = 0,3 (mol)
=> MM = \(\frac{7,2}{0,3}=24\left(\frac{g}{mol}\right)\) ( Mg )
Vậy M là Magie ( Mg )
b) PTHH: xM + yH2SO4 \(\rightarrow\) Mx(SO4)y + yH2 \(\uparrow\)
n\(H_2\) = \(\frac{13,44}{22,4}=0,6\left(mol\right)\)
Theo PT: nM = \(\frac{x}{y}\)n\(H_2\) = \(\frac{0,6x}{y}\)(mol)
=> MM = \(\frac{10,8}{\frac{0,6x}{y}}=\frac{18y}{x}\left(\frac{g}{mol}\right)\)
Ta có bảng sau:
Vậy M là Al
a) nH2= 6.72/22.4=0.3 mol
M + 2HCl --> MCl2 + H2
0.3__________________0.3
mM= 0.3 M = 7.2
<=> M= 24 (Mg)
Vậy: M là magie
b) gọi: hóa trị của M là :n
nH2= 13.44/22.4=0.6 mol
2M + nH2SO4 --> M2(SO4)n + nH2
1.2/n______________________0.6
mM= 1.2/n*M= 10.8
<=> M=9n
Biện luận:
n=1 => M=9 (l)
n=2 => M=18 (l)
n=3 => M=27 (Al)
Vậy: M là Nhôm
Mình sửa lại bài này nhé cậu