1: Cho 300 ml dung dịch glucozơ lên men rượu thu được 13,8 g rượu etylic
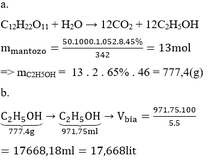
a) tính khối lượng glucozơ tham gia phản ứng và nồng độ mol của dung dịch glucozơ
b) tính độ rượu (thể tích dung dịch coi như không thay đổi khối lượng riêng của rượu etylic nguyên chất bằng 0,8 gam /ml)
c) nếu hiệu suất phản ứng là 95% thì khối lượng glucozơ phải dùng là bao nhiêu?

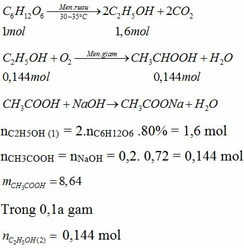

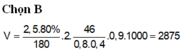
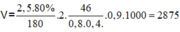
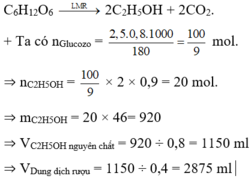
C6H12O6 => (men rượu,to) 2CO2 + 2C2H5OH
nC2H5OH = m/M = 13.8/46 = 0.3 (mol)
Theo phương trình => nC6H12O6 = 0.15 (mol)
mC6H12O6 = n.M = 180 x 0.15 = 27 (g)
300 ml dung dịch = 0.3 l dung dịch
CMddC6H12O6 = n/V = 0.15/0.3 = 0.5M
V = m/D = 13.8/0.8 = 17.25 (ml)
Dr = 17.25x100/300 = 5.75o
mC6H12O6 = 27 x 100/95 = 28.42 (g)
nC2H5OH= 13.8/46= 0.3 mol
C6H12O5 -mr-> 2C2H5OH + 2CO2
0.15___________0.3
mC6H12O6= 0.15*180=27g
CM C6H12O6= 0.15/0.3= 0.5M
300ml= 0.3l
Vdd C2H5OH= m/D= 13.8/0.8= 17.25 ml
Dr= Vdd C2H5OH/ vhh r *100%= 17.25/ 300 *100= 5.75o
mC6H12O= 27*100/95= 28.42g