Ngâm một lá đồng trong 20 ml dung dịch bạc nitrat cho tới khi đồng không thể tan thêm được nửa. Lấy lá đồng ra, rửa nhẹ, làm khô và cân thì thấy khối lượng lá đồng tăng thêm 1,52 gam. Hãy xác định nồng độ mol của dung dịch bạc nitrat đã dùng (giả thiết toàn bộ lượng bạc giải phóng bám hết vào lá đồng)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cu → 2Ag
1 2 → mtang = 2.108-64 = 152g
x 2x → mtang = =1,52g
⇒ x = 1,52/152 = 0,01 mol
⇒ n A g N O 3 = n A g = 2x = 0,02 mol
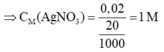
⇒ Chọn C.

PTHH: Cu + 2AgNO3 → Cu(NO3)2 + 2Ag ↓
Theo PTHH: 1 mol Cu tác dụng với 2 mol AgNO3 thì khối lượng tăng 152g.
x mol Cu tác dụng với y mol AgNO3 tăng 1,52g.
=> x = 0,02 mol AgNO3.
Nồng độ dung dịch AgNO3: CMAgNO3 = n/V = 0,02/0,02 = 1(M).
Giải cách này nhé:
Cu+2AgNO3\(\rightarrow\)Cu(NO3)2+2Ag
- Gọi số mol Cu phản ứng là x\(\rightarrow\)số mol Ag tạo thành là 2x
- Độ tăng khối lượng lá Cu=khối lượng Ag sinh ra bám vào Cu- khối lượng Cu bị mất đi do phản ứng. Tức là:
108.2x-64x=1,52\(\rightarrow\)152x=1,52\(\rightarrow\)x=0,01mol
Số mol AgNO3=2x=0,02mol
\(C_{M_{AgNO_3}}=\dfrac{n}{v}=\dfrac{0,02}{0,02}=1M\)

Bài 1:
\(PTHH:Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\\ \Rightarrow n_{Ag}=2n_{Cu}\\ m_{tăng}=m_{Ag}-m_{Cu}=15,2\left(g\right)\\ \Rightarrow108n_{Ag}-64n_{Cu}=15,2\\ \Rightarrow216n_{Cu}-64n_{Cu}=15,2\\ \Rightarrow n_{Cu}=0,1\left(mol\right)\\ \Rightarrow n_{AgNO_3}=0,2\left(mol\right)\\ \Rightarrow C_{M_{AgNO_3}}=\dfrac{0,2}{0,5}=0,4M\)
Bài 2:
\(n_A=\dfrac{78}{M_A}\left(mol\right);n_{ACl}=\dfrac{149}{M_A+35,5}\left(mol\right)\\ PTHH:2A+Cl_2\rightarrow2ACl\\ \Rightarrow n_A=n_{ACl}\Rightarrow\dfrac{78}{M_A}=\dfrac{149}{M_A+35,5}\\ \Rightarrow78M_A+2769=149M_A\\ \Rightarrow71M_A=2769\\ \Rightarrow M_A=39\\ \Rightarrow A\text{ là kali }\left(K\right)\)
Bài 3:
\(a,2Al+3ZnSO_4\rightarrow Al_2\left(SO_4\right)_3+3Zn\\ b,Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ MgO+H_2SO_4\rightarrow MgSO_4+H_2O\\ MgCO_3+H_2SO_4\rightarrow MgSO_4+H_2O+CO_2\uparrow\)

\(a,PTHH:Cu+2AgNO_3\to Cu(NO_3)_2+2Ag\\ b,\text{Đặt } n_{AgNO_3}=x(mol)\\ \Rightarrow n_{Ag}=x;n_{Cu}=\dfrac{1}{2}x\\ \Rightarrow 108x-32x=1,52\\ \Rightarrow x=0,02(mol)\\ \Rightarrow C_{M_{AgNO_3}}=\dfrac{0,02}{ 0,02}=1M\)
\(c,V_{Cu(NO_3)_2}=20(ml)\\ \Rightarrow m_{dd_{Cu(NO_3)_2}}=20.1,1=22(g)\\ n_{Cu(NO_3)_2}=0,01(mol)\\ \Rightarrow m_{Cu(NO_3)_2}=0,01.188=1,88(g)\\ \Rightarrow C\%_{Cu(NO_3)_2}=\dfrac{1,88}{22}.100\%=8,55\%\)

Một hợp chất khí, phân tử có 85,7% C về khối lượng, còn lại là H. Phân tử khối của hợp chất là 28. Tìm số nguyên tử của mỗi nguyên tố trong 1 phân tử hợp chất.