1)Cho 2,7g Al phản ứng với 200ml dd FeSO4 1M.Sau khi phản ứng xảy ra hoàn toàn cho biết :
a. Chất nào hết,chất nào dư.
b.Tính khối lượng Fe thu được(giả sử toàn bộ lượng Fe thu được đều bám trên thanh Al)
c.Dung dịch sau phản ứng gồm những chất nào.Tính CM từng chất trong dd.
2)Trung hòa 20ml dd H2SO41M bẳng dd NaOH 20%.
a.Viết PTHH
b.Tính khối lượng dd H2SO4 cần dùng.
c.Nếu trung hòa dd H2SO4 ở trên bằng dd KOH 5,6%,có khối lượng riêng là 1,045g/ml thì cần bao nhiêu ml dd KOH.

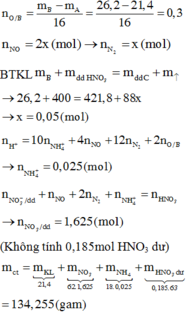

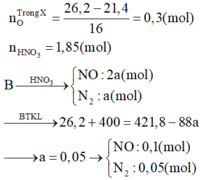

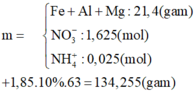
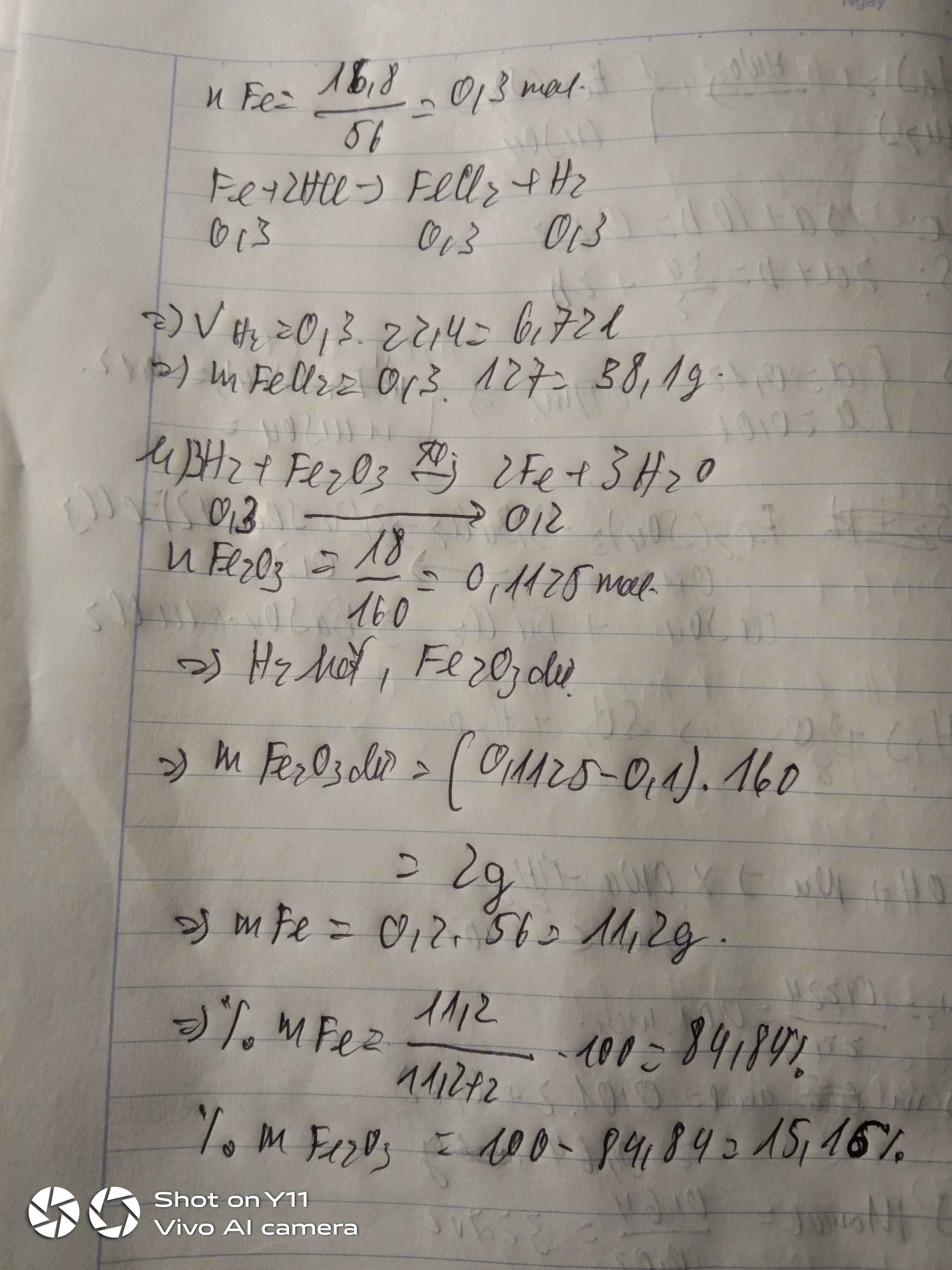

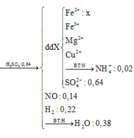
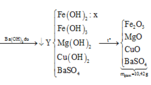
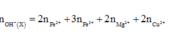

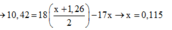
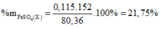
bài 2 là tính NaOH cần dùng chứ sao lại tính H2SO4 cần dùng?