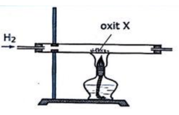
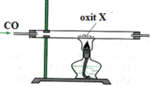
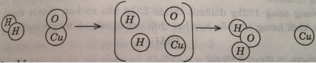Hình bên là sơ đồ thí nghiệm CO phản ứng với oxit kim loại. a) Y có thể là oxit kim loại nào sau đây: CuO, Al2O3, Na2O, Fe3O4, PbO? Viết phương trình hóa học xảy ra. b) Hiện tượng gì xảy ra khi dẫn khí Z vào cốc chứa dung dịch Ca(OH)2 dư. Viết phương trình hóa học xảy ra. |
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
H2 chỉ khử được oxit của kim loại sau Al trong dãy hoạt động hóa học

Những oxit bị khử là: Fe3O4, CuO
Pt: Fe3O4 + 4H2 → 3Fe + 4H2O
CuO + H2 → Cu + H2O
Chú ý: Nhiệt luyện là phương pháp dùng (H2, CO) khử các oxit kim loại trung bình (–K, Na, Ca, Ba, Mg, Al)

a, PTHH:
Fe2O3 + 3H2 ---to---> 2Fe + 3H2O (1)
CuO + H2 ---to---> Cu + H2O (2)
b, nFe = \(\dfrac{2,8}{56}=0,05\left(mol\right)\)
nCu = \(\dfrac{6-2,8}{64}=0,05\left(mol\right)\)
Theo pt (1): nH2 (1) = 2nFe = 2 . 0,05 = 0,1 (mol)
Theo pt (2): nH2 (2) = nCu = 0,05 (mol)
=> VH2 = (0,1 + 0,05) . 22,4 = 3,36 (l)
c, Theo pt (1): nCuO = nCu = 0,05 (mol)
Theo pt (2): nFe2O3 = \(\dfrac{1}{2}n_{Fe}=\dfrac{1}{2}.0,05=0,025\left(mol\right)\)
=> m = 0,05 . 80 + 0,025 . 160 = 8 (g)
\(a.CuO+H_2-^{t^o}\rightarrow Cu+H_2O\\ Fe_2O_3+3H_2-^{t^o}\rightarrow2Fe+3H_2O\\ b.m_{Cu}=6-2,8=3,2\left(g\right)\\ n_{Cu}=0,05\left(mol\right);n_{Fe}=0,05\left(mol\right)\\ \Sigma n_{H_2}=n_{Cu}+\dfrac{3}{2}n_{Fe}=0,125\left(mol\right)\\ \Rightarrow V_{H_2}=2,8\left(l\right)\\ c.n_{CuO}=n_{Cu}=0,05\left(mol\right);n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe}=0,025\left(mol\right)\\ m_{hh}=m_{CuO}+m_{Fe_2O_3}=0,05.80+0,025.160=8g\)

\(\left(K_2O,Al_2O_3,BaO\right)\underrightarrow{H_2O}\left(KOH,Ba\left(OH\right)_2\right),\left(Al_2O_3\right)\\ \left(Al_2O_3\right)\underrightarrow{dpnc}Al\\ \left(KOH,Ba\left(OH\right)_2\right)\underrightarrow{KHCO_3}\left(K_2CO_3,KHCO_3\right),\left(BaCO_3\right)\\ \left(BaCO_3\right)\underrightarrow{HCl}BaCl_2\underrightarrow{dp}Ba\\ \left(K_2CO_3,KHCO_3\right)\underrightarrow{HCl}\left(KCl\right)\underrightarrow{dp}K\\ K_2O+H_2O->2KOH\\ BaO+H_2O->Ba\left(OH\right)_2\\ Al_2O_3-dpnc->2Al+\dfrac{3}{2}O_2\\ KOH+KHCO_3->K_2CO_3+H_2O\\ Ba\left(OH\right)_2+2KHCO_3->BaCO_3+K_2CO_3+2H_2O\\ BaCO_3+2HCl->BaCl_2+H_2O+CO_2\\ BaCl_2-dp->Ba+Cl_2\\ K_2CO_3+2HCl->2KCl+H_2O+CO_2\\ KHCO_3+HCl->KCl+H_2O+CO_2\\ KCl-dp->K+\dfrac{1}{2}Cl_2\)

Mỗi phản ứng xảy ra với 1 phân tử H 2 và 1 phân tử CuO, tạo ra 1 phân tử H 2 O và 1 nguyên tử Cu.