cho hỗn hợp 10,8 gam bột cu và fe vào lượng dư h2so4 đặc . thu được 2,24 lít khí so2 . tính phần trăm mỗi kim loại trong hỗn hợp .
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
Gọi a, b lần lượt là số mol của Fe, Cu
56a + 64b = 14,8 (1)
Quá trình nhường electron:
Fe - 3e → Fe
a 3a
Cu - 2e → Cu
b 2b
→ ∑ne nhường = (3a + 2b) mol
Quá trình nhận electron:
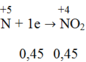
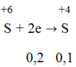
→ ∑ne nhận = 0,45 + 0,2 = 0,65 mol
Áp dụng định luật bảo toàn electron:
3a + 2b = 0,65 → a = 0,15 và b = 0,1 → mFe = 8,4 g

Mg + 2 H2SO4 (đ) -to-> MgSO4 + SO2 + 2 H2O
x_________2x__________________x(mol)
2 Fe + 6 H2SO4(đ) -to-> Fe2(SO4)3 + 3 SO2 + 6 H2O
y______3y_____________________1,5y(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}24x+56y=18,4\\x+1,5y=0,6\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,3\\y=0,2\end{matrix}\right.\)
=> mMg= 0,3.24=7,2(g)
=> %mMg= (7,2/18,4).100=39,13%
=>%mFe= 60,87%
b) nH2SO4(tổng)=2x+3y=2.0,3+3.0,2=1,2(mol)
VddH2SO4=1,2/2=0,6(l)
a) Đặt \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Mg}=b\left(mol\right)\end{matrix}\right.\) \(\Rightarrow56a+24b=18,4\) (1)
Ta có: \(n_{SO_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
Bảo toàn electron: \(3a+2b=0,6\cdot2\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,2\\b=0,3\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,2\cdot56}{18,4}\cdot100\%\approx60,87\%\\\%m_{Mg}=39,13\%\end{matrix}\right.\)
b) Ta có: \(\left\{{}\begin{matrix}n_{Fe_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Fe}=0,1\left(mol\right)\\n_{MgSO_4}=n_{Mg}=0,3\left(mol\right)\end{matrix}\right.\)
Bảo toàn nguyên tố: \(n_{H_2SO_4}=n_{SO_2}+3n_{Fe_2\left(SO_4\right)_3}+n_{MgSO_4}=1,2\left(mol\right)\)
\(\Rightarrow V_{H_2SO_4}=\dfrac{1,2}{2}=0,6\left(l\right)=600\left(ml\right)\)

a) nNO=8,96/22,4=0,4(mol)
bảo toàn e:
Al0 --> Al3+ +3e
x 3x
Cu0--> cu+2+ + 2e
y 2y
N+5 + 3e --> N+2
1,2 0,4
=> hệ: 27x+64y=24,6 và 3x+2y=1,2
bấm máy ta được: x= 0,2 và y=0,3
=> mAl=5,4g ; mCu=19,2g
b) Al + 4HNO3 --> Al(NO3)3 + NO + 2H2O
3Cu + 8HNO3 --> 3Cu(NO3)2 + 2NO + 4H2O
Ta thấy: nHNO3(phản ứng)=4nNO=1,6(mol)
=> nHNO3(đã dùng)=1,6+1,6*20%=1,92(mol)
=>VHNO3(đã dùng)=1,92/1=1,92(l)

a, Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH:
Fe + 2HCl ---> FeCl2 + H2
a--->2a------------------>a
2Al + 6HCl ---> 2AlCl3 + 3H2
b---->3b-------------------->1,5b
=> \(\left\{{}\begin{matrix}56a+27b=16,6\\a+1,5b=0,5\end{matrix}\right.\Leftrightarrow a=b=0,2\left(mol\right)\)
=> \(\left\{{}\begin{matrix}m_{Fe}=0,2.56=11,2\left(g\right)\\m_{Al}=0,2.27=5,4\left(g\right)\end{matrix}\right.\)
b) \(C\%_{HCl}=\dfrac{\left(0,2.2+0,2.3\right).36,5}{300}.100\%=12,167\%\)
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
gọi nFe : a , nAl: b (a,b>0) => 56a + 27b = 16,6 (g)
\(pthh:Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
a a
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
b \(\dfrac{3b}{2}\)
=> \(a+\dfrac{3b}{2}=0,5\)
ta có hệ pt
\(\left\{{}\begin{matrix}56a+27b=16,6\\a+\dfrac{3b}{2}=0,5\end{matrix}\right.\)
=> a= 0,2 , b = 0,2
\(\left\{{}\begin{matrix}m_{Fe}=0,2.56=11,2\left(g\right)\\m_{Al}=16,6-11,2=5,4\left(g\right)\end{matrix}\right.\)
\(pthh:Fe+2HCl\rightarrow FeCl_2+H_2\)
0,2 0,4
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,2 0,6
=> \(m_{HCl}=\left(0,4+0,6\right).36,5=36,5\left(g\right)\)
=> \(C\%=\dfrac{36,5}{200}.100\%=18,25\%\)

Đáp án B
Ta có:
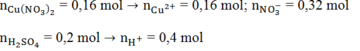
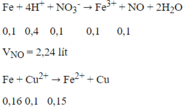
Do Fe nên tiếp tục xảy ra phản ứng:

nFe phản ứng = 0,1 + 0,05 + 0,16 = 0,31 mol
0,6m (g) hỗn hợp bột kim loại sau phản ứng gồm Fe dư và Cu sinh ra:
m - mFe pư + mCu = 0,6m → m - 0,31.56+ 64.0,16 = 0,6m
m = 17,8 (g)

1.1. Al + NaOH + H2O ==> NaAlO2 + 3/2H2
nH2(1)=3,36/22,4=0.15(mol)
=> nAl(1)= nH2(1):3/2= 0.15:3/2= 0.1(mol)
2.Mg + 2HCl ==> MgCl2 + H2
3.2Al + 6HCl ==> 2AlCl3 + 3H2
4.Fe + 2HCl ==> FeCl2 + H2
=> \(n_{H_2\left(2,3,4\right)}=\) 10.08/22.4= 0.45(mol)
=> nH2(3)=0.1*3/2=0.15(mol)
MgCl2 + 2NaOH ==> Mg(OH)2 + 2NaCl
AlCl3 + 3NaOH ==> Al(OH)3 + 3NaCl
FeCl2 + 2NaOH ==> Fe(OH)2 + 2NaCl

\(n_{SO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
Mol: x x
PTHH: Fe + 2H2SO4 → FeSO4 + SO2 + 2H2O
Mol: y y
Ta có: \(\left\{{}\begin{matrix}64x+56y=10,8\\x+y=0,1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,65\\y=-0,55\end{matrix}\right.\left(đềsai\right)\)