Đốt cháy 0,15 mol hỗn hợp : metyl acrylat, etylen glicol, anddehit axetic, ancol metylic cần x mol O2, sau phản ứng thu được 0,38 mol CO2 . Gía trị của x là?
Bài này ở mức độ lấy điểm 8 trong đề thi THPT quốc gia
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C
☆ dạng bài tập đốt cháy thuần (không quan tâm đến tính chất hóa học của các chất đem đốt).
→ chúng ta cũng chỉ cần xem xét CTPT của nó thôi: 0,15 mol hỗn hợp gồm
C4H6O2 (metyl acrylat) C2H6O2 (etylen glicol); C2H4O (axetanđehit) và CH4O (ancol metylic).
Yêu cầu x mol O2 cần để đốt, giả thiết 0,38 mol CO2
→ bỏ cụm "H2O".
C4H6O2 = 4C + 1H2 + 2H2O;
C2H6O2 = 2C + 1H2 + 2H2O.
C2H4O = 2C + 1H2 + 1H2O;
CH4O = 1C + 1H2 + 1H2O.
YTHH 01: 0,15 mol hỗn hợp quy về hỗn hợp gồm:
0,38 mol C + 0,15 mol H2 + ??? mol H2O
không quan tâm H2O vì nó không cần O2 để đốt (mà quan tâm cũng không tính được).
C + O2 → CO2;
2H2 + O2 → 2H2O
→ ∑ n O 2 c ầ n = 0 , 38 + 0 , 15 ÷ 2 = 0 , 455 m o l

Chọn D
Từ thông tin đề cho ta có thể tìm được số mol của CO2. Để tìm được mol O2 tham gia phản ứng đốt cháy hỗn hợp X thì cần tìm số mol H trong X tham gia phản ứng cháy. Nhưng số H trong X của các hợp chất lại rất khác nhau. Khó quá !Làm thế nào đây ?
Ta thử làm như sau :
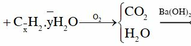
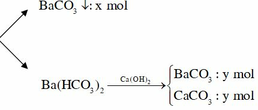


Đáp án A
CO2 + Ba(OH)2 → BaCO3 + H2O (1)
CO2 + Ba(OH)2 → Ba(HCO3)2 (2)
Ba(HCO3)2 + Ca(OH)2→ BaCO3 + CaCO3 + H2O (3)
Gọi số mol ở (3) của CaCO3 = BaCO3 = x (mol)
=> 100x + 197x = 53,46
=> x = 0,18 (mol)
Bảo toàn nguyên tố Ba => nBaCO3(1) = 0, 2- 0,18 = 0,02 (mol)
Bảo toàn nguyên tố C => nCO2 = nBaCO3(1) + 2nBa(HCO3)2 = 0,38 (mol)
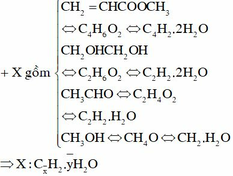
CH2 = CH – COOCH3 hay C4H6O2 = C4H2 + 2H2O
HO-CH2-CH2-OH hay C2H6O2 = C2H2 + 2H2O
CH3-CHO hay C2H4O = C2H2 + H2O
CH3OH hay CH4O = CH2 + H2O
Vậy phần cháy được có công thức chung là CxH2: 0,15 (mol)
CxH2 + (x + 0,5) O2 → xCO2 + H2O
0,15 →0,15 ( x + 0,5) →0,38
=> x = 0,38 / 0,15
=> nO2 = 0,15 ( x + 0,15 ) = 0,445 (mol)

Đáp án A
CO2 + Ba(OH)2 → BaCO3 + H2O (1)
CO2 + Ba(OH)2 → Ba(HCO3)2 (2)
Ba(HCO3)2 + Ca(OH)2→ BaCO3 + CaCO3 + H2O (3)
Gọi số mol ở (3) của CaCO3 = BaCO3 = x (mol)
=> 100x + 197x = 53,46
=> x = 0,18 (mol)
Bảo toàn nguyên tố Ba => nBaCO3(1) = 0, 2- 0,18 = 0,02 (mol)
Bảo toàn nguyên tố C => nCO2 = nBaCO3(1) + 2nBa(HCO3)2 = 0,38 (mol)
CH2 = CH – COOCH3 hay C4H6O2 = C4H2 + 2H2O
HO-CH2-CH2-OH hay C2H6O2 = C2H2 + 2H2O
CH3-CHO hay C2H4O = C2H2 + H2O
CH3OH hay CH4O = CH2 + H2O
Vậy phần cháy được có công thức chung là CxH2: 0,15 (mol)
CxH2 + (x + 0,5) O2 → xCO2 + H2O
0,15 →0,15 ( x + 0,5) →0,38
=> x = 0,38 / 0,15
=> nO2 = 0,15 ( x + 0,15 ) = 0,445 (mol)

Đáp án A
CO2 + Ba(OH)2 → BaCO3 + H2O (1)
CO2 + Ba(OH)2 → Ba(HCO3)2 (2)
Ba(HCO3)2 + Ca(OH)2→ BaCO3 + CaCO3 + H2O (3)
Gọi số mol ở (3) của CaCO3 = BaCO3 = x (mol)
=> 100x + 197x = 53,46
=> x = 0,18 (mol)
Bảo toàn nguyên tố Ba => nBaCO3(1) = 0, 2- 0,18 = 0,02 (mol)
Bảo toàn nguyên tố C => nCO2 = nBaCO3(1) + 2nBa(HCO3)2 = 0,38 (mol)
CH2 = CH – COOCH3 hay C4H6O2 = C4H2 + 2H2O
HO-CH2-CH2-OH hay C2H6O2 = C2H2 + 2H2O
CH3-CHO hay C2H4O = C2H2 + H2O
CH3OH hay CH4O = CH2 + H2O
Vậy phần cháy được có công thức chung là CxH2: 0,15 (mol)
CxH2 + (x + 0,5) O2 → xCO2 + H2O
0,15 →0,15 ( x + 0,5) →0,38
=> x = 0,38 / 0,15
=> nO2 = 0,15 ( x + 0,15 ) = 0,445 (mol)

Chọn đáp án A
Hỗn hợp gồm: C4H6O2; C2H6O2; C2H4O và CH4O.
Quan sát: 2 thằng đầu cùng H6O2; 2 thằng sau cùng H4O.
Yêu cầu liên quan đến O2 cần đốt
→ tách bỏ H2O lại thấy sự đặc biệt:
0,15 mol hỗn hợp gồm x mol C + y mol H2O + 0,15 mol H2.
♦ Chuyển qua bài tập CO2 + dung dịch kiềm: vì Ca(OH)2 vào có thêm kết tủa
→ C O 2 + 0 , 2 m o l B a ( O H ) 2 → B a C O 3 ↓ + B a H C O 3 2 1
Theo đó: C a ( O H ) 2 + B a H C O 3 2 → C a C O 3 + B a C O 3 + 2 H 2 O 2
mtủa (2) = 18 gam→ có 0,18 mol Ca(HCO3)2 và 0,18 mol BaCO3. Bảo toàn Ba → n B a C O 3 ở ( 1 ) = 0 , 02 m o l
→ x = ∑ n C O 2 = 0 , 02 + 0 , 18 × 2 = 0 , 38 m o l (theo bảo toàn C ở (1)).
► để ý yêu cầu: H2O không cần O2 để đốt → không quan tâm đến y mà
có luôn: a = ∑ n O 2 c ầ n đ ố t = x + 1 2 n H 2 = 0 , 38 + 0 , 15 ÷ 2 = 0 , 455 m o l