Hòa tan hoàn toàn 0,65 gam kẽm vào 50ml dung dịch axit clohiđric thu được sản phẩm là muối kẽm Clorua và khí hidro a, viết phương trình hóa học b, tính khối lượng muối kẽm clorua c, tính nồng độ mol của dung dịch axit clohiđric d, tính thể tích khí hidro ở đktc
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) Lập công thức hóa học của muối kẽm clorua: Z n C l 2
b) Khối lượng muối Z n C l 2 = 6,5 + 7,3 – 0,2 = 13,6 (gam)

a. Zn + 2HCl → ZnCl2 + H2
b. nZn = n\(_{ZnCl_2}\) =\(\dfrac{13}{65}=0,2\left(mol\right)\) => m\(_{ZnCl_2}\)= 0,2.136 = 27,2(g)
c. n\(_{H_2}\)= nZn = 0,2 (mol) => V\(_{H_2}\)=0,2.22,4 = 4,48 (lít)

a)
\(Zn + 2HCl \to ZnCl_2 + H_2\)
b),c)
Theo PTHH :
\(n_{ZnCl_2} = n_{H_2} = n_{Zn} = \dfrac{13}{65} = 0,2(mol)\)
Vậy :
\(m_{ZnCl_2} = 0,2.136 = 27,2(gam)\\ V_{H_2} =0,2.22,4 = 4,48(lít)\)

a. \(n_{Zn}=\dfrac{6.5}{65}=0,1\left(mol\right)\)
PTHH : Zn + 2HCl -> ZnCl2 + H2
0,1 0,2 0,1
b. \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c. \(m_{HCl}=0,2.36,5=7,3\left(g\right)\)
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
\(m_{HCl}=0,2\cdot36,5=7,3g\)

a,\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl ---> ZnCl2 + H2
0,1--------------->0,1------>0,1
b, => \(\left\{{}\begin{matrix}C_{M\left(ZnCl_2\right)}=\dfrac{0,1}{\dfrac{6}{1000}}=\dfrac{50}{3}M\\V_{H_2}=0,1.22,4=2,24\left(l\right)\end{matrix}\right.\)
c, \(n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: 2H2 + O2 --to--> 2H2O
LTL: \(\dfrac{0,1}{2}< 0,1\)=> O2 dư
Theo pt: \(n_{O_2}=\dfrac{1}{2}n_{H_2}=\dfrac{1}{2}.0,1=0,05\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{O_2\left(dư\right)}=\left(0,1-0,05\right).32=1,6\left(g\right)\\V_{O_2\left(dư\right)}=\left(0,1-0,05\right).22,4=1,12\left(l\right)\end{matrix}\right.\)

a.b.c.\(n_{Zn}=\dfrac{m}{M}=\dfrac{13}{65}=0,2mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2 0,2 0,2 ( mol )
\(m_{ZnCl_2}=n.M=0,2.136=27,2g\)
\(V_{H_2}=n.22,4=0,2.22,4=4,48l\)
d.\(n_{CuO}=\dfrac{m}{M}=\dfrac{32}{80}=0,4mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,4 > 0,2 ( mol )
0,2 0,2 0,2 ( mol )
\(m_{chất.rắn}=m_{CuO\left(dư\right)}+m_{Cu}=0,2.80+0,2.64=16+12,8=28,8g\)
\(\%m_{CuO}=\dfrac{16}{28,8}.100=55,55\%\)
\(\%m_{Cu}=100\%-55,55\%=44,45\%\)

\(n_{Zn}=\dfrac{3,25}{65}=0,05mol\)
a)\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,05 0,1 0,05 0,05
b)\(m_{ZnCl_2}=0,05\cdot136=6,8g\)
c)\(V_{H_2}=0,05\cdot22,4=1,12l\)
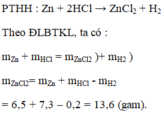
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
Ta có: \(n_{Zn}=\dfrac{0,65}{65}=0,01\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=0,02\left(mol\right)\\n_{ZnCl_2}=0,01\left(mol\right)=n_{H_2}\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C_{M_{HCl}}=\dfrac{0,02}{0,05}=0,4\left(M\right)\\m_{ZnCl_2}=0,01\cdot136=1,36\left(g\right)\\V_{H_2}=0,01\cdot22,4=0,224\left(l\right)\end{matrix}\right.\)