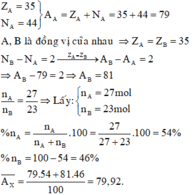1. Trong tự nhiên, Y có 2 đồng vị bền là A135Y và A2ZY. Phần trăm số nguyên tử của đồng vị A135Y là 54%, còn lại là của đồng vị A2ZY. Đồng vị A135Y có 44n và đồng vị A2ZY hơn đồng vị A135Y là 2 nơtron. Tính nguyên tử khối trung bình của Y.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn A
Gọi % số nguyên tử của đồng vị C 6 13 là x %, thì % số nguyên tử của đồng vị C là 100 – x (%).
Ta có
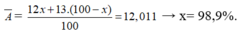

a) Đặt %24Mg là x
-->%25Mg là (100 - x - 11)
\(\overline{M}=\dfrac{x.24+\left(100-x-11\right).25+11.26}{100}=24,32\)
\(\Rightarrow x=\%^{24}Mg=79\%\)
b) ta có : \(n_{Mg}=n_{MgCl2}=1\left(mol\right)\Rightarrow n_{26_{Mg}}=1.11\%=0,11\left(mol\right)\)
Số nguyên tử : \(0,11.6,022.10^{-3}=6,6022.10^{-4}\)(nguyên tử)

Đáp án A
Gọi số khối của đồng vị X, Y lần lượt là x, y
Chú ý Số nguyên tử đồng vị X = 0,37 số nguyên tử đồng vị Y nên nếu có 1 nguyên tử Y thì có 0,37 nguyên tử X
Ta có hệ:
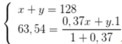
⇒
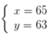
Vậy số notron của đồng vị Y hơn số notron của đồng vị X là : 65- 63 = 2

Chọn A
Gọi % của đồng vị 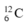 là x, thì % của đồng vị
là x, thì % của đồng vị 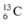 là 100 - x
là 100 - x
Ta có
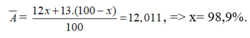 .
.