Hòa tan 3,84 gam kim loại Mg vào V lít dung dịch HNO3 0,25 m vừa đủ thu được dung dịch X và và 0,448 lít một chất khí Y duy nhất nguyên chất cô cạn cẩn thận dung dịch X thu được 25,28 g muối khan quá trình cô cạn không làm muối phân hủy Giá trị của V là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nMg= 0,07 mol=nMg(NO3)2 → mMg(NO3)2= 0,07. 148= 10,36 gam≠ 11,16 gam
→Muối khan phải chứa cả Mg(NO3)2 và NH4NO3
mNH4NO3=11,16- 10,36= 0,8 gam →nNH4NO3= 0,01 mol
Quá trình cho e:
Mg→ Mg2++ 2e (1)
0,07→ 0,14 mol
Quá trình nhận e: nkhí= 0,02mol
NO3-+ 8e + 10H+ → NH4+ + 3H2O (2)
0,08 0,1 0,01 mol
-Nếu khí có 1 nguyên tử N:
N+5 + (5-a) e→ N+a
(5-a).0,02 0,02
Theo ĐL bảo toàn electron có: 0,14= 0,02. (5-a)+0,08→ a= 2 → NO
-Nếu khí có 2 nguyên tử N:
2N+5 + 2(5-a) e→ N2+a
(5-a).0,04 0,02
Theo ĐL bảo toàn electron có: 0,14= 0,04. (5-a) + 0,08→ a= 3,5 loại
Ta có:
NO3-+ 3e+4H+→ NO+ 2H2O (3)
0,06 0,08 0,02 mol
Theo các bán phản ứng (2) và (3)
nH+= 10nNH4++ 4.nNO= 10.0,01+ 4.0,02= 0,18 mol=nHNO3
→V= 0,18/0,25= 0,72 lít
Đáp án B

=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=-=

Bảo toàn nguyên tố Mg ta có:
nMg(NO3)2= 0,2+ 0,03= 0,23 mol → mMg(NO3)2= 0,23. 148= 34,04 gam≠ 34,84 gam
→Muối khan phải chứa cả Mg(NO3)2 và NH4NO3
mNH4NO3=34,84- 34,04= 0,8 gam →nNH4NO3= 0,01 mol
Quá trình cho e:
Mg→ Mg2++ 2e (1)
0,2→ 0, 4 mol
Quá trình nhận e: nkhí= 0,04mol
NO3-+ 8e + 10H+ → NH4+ + 3H2O (2)
0,08 0,1 0,01 mol
-Nếu khí có 1 nguyên tử N: Gọi a là số oxi hóa của N có trong khí
N+5 + (5-a) e→ N+a
(5-a).0,04 0,04
Theo ĐL bảo toàn electron có: 0,4= 0,04. (5-a)+0,08→ a= -3 → Loại
-Nếu khí có 2 nguyên tử N:
2N+5 + 2(5-a) e→ N2+a
(5-a).0,08 0,04
Theo ĐL bảo toàn electron có: 0, 4= 0,08. (5-a) + 0,08→ a= 1→Khí N2O
Đáp án B

Đáp án B
(*) Phương pháp: Bảo toàn e, Bảo toàn khối lượng
- Lời giải: Vì KL +HNO3 không có khí thoát ra sản phẩm khử là NH4NO3
TQ:
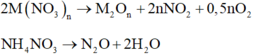
nO(x) = 0,61364m /16(mol)
![]()
Ta có
![]()
![]()
![]()
Bảo toàn khối lượng mX – mran = mNH4NO3 + mNO2 + mO2
![]()
![]()

Giải thích:
Vì KL + HNO3 không có khí thoát ra => sản phẩm khử là NH4NO3
TQ : 2M(NO3)n ---> M2On + 2nNO2 + 0,5nO2
NH4NO3 ---> N2O + 2H2O
nO(X) = 0,61364m/16 (mol)
nNO3 = ne tđ + nNH4NO3 = 1/3nO(X) = 0,61364m/48 (mol)
Ta có : ne tđ = 8nNH4NO3
=> ne tđ = 0,61364m/54 = nNO2 = 4nO2 ; nNH4NO3 = 0,61364m/432
=> nO2 = 0,61364m/216 (mol)
Bảo toàn khối lượng : mX - mrắn = mNH4NO3 + mNO2 + mO2
=> m – 19,2 = 80. 0,61364m/432 + 46. 0,61364m/54 + 32. 0,61364m/216
=> m = 70,4g
Đáp án B

Đáp án B
(*) Phương pháp: Bảo toàn e, Bảo toàn khối lượng
- Lời giải: Vì KL + H N O 3 không có khí thoát ra
⇒ sản phẩm khử là N H 4 N O 3
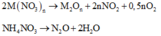
n O ( X ) = 0 , 61364 m / 16 ( m o l )
n N O 3 = n e t d + n N H 4 N O 3 = 1 3 n O ( X ) = 0 , 61364 / 48 ( m o l )
⇒ n O 2 = 0 , 61364 m / 216 ( m o l )
Bảo toàn khối lượng
m X - m r a n = m N H 4 N O 3 + m N O 2 + m O 2
![]()
⇒ m = 70 , 4 g

Chọn B
2HCl → H2
⇒ nCl = 2nH2 = 2.0,35 = 0,7
⇒ mmuối = (9,14 – 2,54) + 0,7.35,5 = 31,45g


$n_{Mg(NO_3)_2} = n_{Mg} = \dfrac{3,84}{24} = 0,16(mol)$
$\Rightarrow n_{NH_4NO_3} = \dfrac{25,28 - 0,16.148}{80}= 0,02(mol)$
Gọi n là số electron trao đổi của khí Y
Bảo toàn electron :
$0,16.2 = 0,02.8 + 0,02n \Rightarrow n = 8$
Vậy khí Y là $N_2O$
Phân bổ $H^+$ : $n_{HNO_3} = 10n_{N_2O} + 10n_{NH_4NO_3} = 0,4(mol)$
$V = \dfrac{0,4}{0,25} = 1,6(lít)$