Để khử hoàn toàn oxit trong 3,2 gam oxit của kim loại cần 1,344 lít khí H2. Hòa tan lượng kim loại thu được trong dd axit HCl dư thì thu được 0,896 lít khí H2 (các thể tích khí đều đo ở đktc). Giải thích vì sao thể tích hidro trong hai trường hợp không giống nhau và xác định kim loại
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


hòa tan kl trong dd nào hả bạn ? axit hay bazo? Bạn xem lại đề nhá

Đáp án A
Oxit chưa biết của kim loại nào → Gọi MxOy
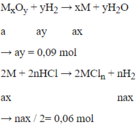
Mà : 56ax + 16ay = 4,8
→ ax = 0,06
→ x : y = ax : ay = 0,06 : 0,09 = 2 : 3 => M2O3
→ n = 0,12 : 0,06 = 2 => M hóa trị II
→ Chỉ có Fe thỏa mãn vì nó có hai hóa trị
Lưu ý: Bài toán này dễ nhầm lẫn nếu không để ý sự thay đổi hóa trị ở 2 phương trình.

Ta có : + H2 --> H2O
0,06-----0,06
--> m(R) = 3,48 - 0,06.16 = 2,52 gam
--> \(\frac{2,25n}{M}=\frac{1,008}{22,4}\)(n là hoá trị của R)
--> 28.n = M
--> n = 2 --> M = 56 (Fe)
nFe : nO = 0,045 : 0,06 = 3 : 4 --> oxit là :

Gọi công thức oxit ban đầu là MxOy.
Có phản ứng khử hoàn toàn oxit MxOy thành kim loại:
![]()
Dẫn khí CO2 sinh ra hấp thụ vào dung dịch Ca(OH)2 dư:
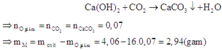
Cần lưu ý: Hóa trị của kim loại M trong oxit ban đầu và hóa trị của M trong sản phẩm của phản ứng giữa M với axit HCl có thể khác nhau.
Do đó ta gọi n là hóa trị của M thể hiện khi phản ứng với axit HCl.
![]()
Áp dụng định luật bào toàn mol electron, ta có:
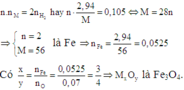
Đáp án D.

Đặt a là hoá trị kim loại M cần tìm (a: nguyên, dương)
\(M_2O_a+aH_2\rightarrow\left(t^o\right)2M+aH_2O\left(1\right)\\ 2M+2aHCl\rightarrow2MCl_a+aH_2\left(2\right)\\Ta.có:n_{H_2\left(2\right)}=\dfrac{1,008}{22,4}=0,045\left(mol\right)\\ n_{H_2\left(1\right)}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\\ \Rightarrow n_{O\left(trong.oxit\right)}=n_{H_2O}=n_{H_2\left(1\right)}=0,06\left(mol\right)\\ \Rightarrow m_M=3,48-0,06.16=2,52\left(g\right)\\ n_{H_2\left(2\right)}=0,045\left(mol\right)\\ \Rightarrow n_{M\left(2\right)}=\dfrac{0,045.2}{a}=\dfrac{0,09}{a}\left(mol\right)\\ \Rightarrow M_M=\dfrac{2,52}{\dfrac{0,09}{a}}=28a\left(\dfrac{g}{mol}\right)\)
Xét các TH: a=1; a=2; a=3; a=8/3 thấy a=2 thoả mãn khi đó MM=56(g/mol), tức M là Sắt (Fe=56)
Đặt CTTQ của oxit sắt cần tìm là FemOn (m,n: nguyên, dương)
\(n_{Fe}=\dfrac{2,52}{56}=0,045\left(mol\right)\\n_O=0,06\left(mol\right)\)
=> m:n= 0,045:0,06=3:4
=>m=3;n=4
=> CTHH oxit: Fe3O4 (Sắt từ oxit)
-Em chỉ mới lập được phương trình hóa học tổng quát thôi, em chưa tính được.

Gọi oxit kim loại là R2On Kim loại này phải có số oxh thay đổi
nCO=1,792/22,4=0,08 mol
R2On + nCO =>2 R + nCO2
0,08/n mol<=0,08 mol=>0,16/n mol
nH2=1,344/22,4=0,06 mol
2R +2mHCl =>2RClm +m H2
0,12/m mol<= 0,06 mol
=>m/n=4/3
Có 0,08/n(2R+16n)=4,64=>R=21n chọn n=8/3=>R=56 Fe
Oxit kim loại là Fe3O4
Gọi công thức oxit kim loại là :MxOy
_Tác dụng với CO:
nCO=1.792/22.4=0.08(mol)
MxOy+yCO=>xM+yCO2
0.08/y->0.08(mol)
=>nMxOy=0.08/y(1)
=>nO=0.08mol
=>mO=0.08*16=1.28(g)
=>mM=4.64-1.28=3.36(g)
nH2=1.344/22.4=0.06(mol)
2M+2nHCl=>2MCln+nH2
0.12/n----------------->0.06(mol)
=>M=3.36/0.12/n=28n
_Xét hóa trị của M từ 1->3:
+n=1=>M=28(loại)
+n=2=>M=56(nhận)
+n=3=>M=84(loại)
=>M là sắt (Fe)
=>nFe=0.12/2=0.06(mol)
=>nFexOy=0.06/x (2)
Từ(1)(2)=>
0.08/y=0.06/x
<=>0.08x=0.06y
<=>x/y=3/4
Vậy công thức oxit đầy đủ là Fe3O4

\(n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\) \(\Rightarrow y=0,03\left(mol\right)\)
\(Fe_xO_y+yH_2\rightarrow\left(t^o\right)xFe+yH_2O\)
\(n_{H_2}=\dfrac{0,448}{22,4}=0,02mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,02 0,02 ( mol )
\(\Rightarrow x=0,02\left(mol\right)\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{0,02}{0,03}=\dfrac{2}{3}\)
\(\Rightarrow CTHH:Fe_2O_3\)
\(n_{H_2\left(thu\right)}=\dfrac{V}{22,4}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
1 : 1 (mol)
0,02 : 0,02 (mol)
\(n_{H_2\left(dùng\right)}=\dfrac{V}{22,4}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
\(yH_2+Fe_xO_y\rightarrow^{t^0}xFe+yH_2O\)
y : x (mol)
0,03 : 0,02 (mol)
\(\Rightarrow\dfrac{0,03}{y}=\dfrac{0,02}{x}\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{0,02}{0,03}=\dfrac{2}{3}\Rightarrow x=2;y=3\)
-Vậy CTHH của oxit sắt là Fe2O3.



Gọi oxit cần tìm là M2On
M2On + nH2 --> 2M + nH2O (1)
Ta có: nH2(1)= 0,06 => nH2O= 0,06
ADĐLBTKL vào pt(1)
3,2 + 0,06x2 = mM + 0,06x18
=> mM = 2,24
2M + 2nHCl --> 2MCln + nH2 (2)
nH2(2) = 0,04 => nM= \(\dfrac{0,08}{n}\)
=> mM = \(\dfrac{0,08.M}{n}\)= 2,24
=> M=28n => M là Fe
Mình nghĩ là thể tích ở 2 THop này ko bằng nhau ví đây là sắt và oxit sắt mà oxit sắt có tới 3 THop cơ nên nó khác nhau(Mình ko chắc đâu nhá)