Phân biệt các chất dựa vào tính chất vật lý :
a) 2 chất bột : AgCl và AgNO3
b) Fe, Cu và AgNO3
c) Cl2, O2 , và CO2
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A. Cu(OH)2 và AgNO3/NH3.
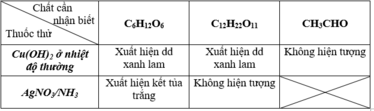
PTHH:
2C6H12O6 + Cu(OH)2 → (C6H11O6)2Cu + 2H2O
2C12H22O11 + Cu(OH)2 → (C12H21O11)2Cu + 2H2O
C5H11O5CHO + 2AgNO3 + 3NH3 + H2O 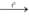 C5H11O5COONH4 + 2Ag + 2NH4NO3
C5H11O5COONH4 + 2Ag + 2NH4NO3
phân biệt các chất sau bằng phương pháp vật lý
a) Fe , Cu , Cuo , S
b) AgNo3 , Cu , Fe
c) KOH , Cu(OH)2

Dựa vào màu sắc:
a)
- Chất rắn màu trắng xám: Fe
- Chất rắn màu đỏ: Cu
- Chất rắn màu đen: CuO
- Chất rắn màu vàng: S
b)
- Chất rắn màu trắng: AgNO3
- Chất rắn màu đỏ: Cu
- Chất rắn màu trắng xám: Fe
c)
- Chất rắn màu trắng: KOH
- Chất rắn màu xanh: Cu(OH)2

Trường hợp Cu dư:
Cu + 2AgNO3 → Cu(NO3)2+ 2Ag ↓
Cu + 2Fe(NO3)3 → Cu(NO3)2 + 2Fe(NO3)2
Rắn A : Ag, Cu dư
Dung dịch B : Cu(NO3)2, Fe(NO3)2

a) m rắn=4,08 gam
b) CM Cu(NO3)2 dư=0,35M; CM Fe(NO3)2=0,2M
c) V NO2=1,792 lít
Giải thích các bước giải:
Ta có: nAgNO3=0,2.0,1=0,02 mol; nCu(NO3)2=0,5.0,2=0,1 mol; nFe=2,24/56=0,04 mol
Fe + 2AgNO3 -> Fe(NO3)2 + 2Ag
Vì nAgNO3=0,02 mol; nFe =0,04 -> Fe dư -> tạo ra 0,02 mol Ag và Fe phản ứng 0,01 mol -> dư 0,03 mol
Fe + Cu(NO3)2 -> Fe(NO3)2 + Cu
Vì Cu(NO3)2=0,1 mol; nFe =0,03 mol -> Cu(NO3)2 dư =0,07 mol ; nCu=0,03 mol
Rắn thu được gồm Ag 0,02 mol và Cu 0,03 mol -> m rắn=4,08 gam
Dung dịch sau phản ứng chứa Cu(NO3)2 dư 0,07 mol và Fe(NO3)2 0,04 mol (Bảo toàn Fe)
-> CM Cu(NO3)2=0,07/0,2=0,35M; CM Fe(NO3)2=0,04/0,2=0,2M
Hòa tan rắn bằng HNO3 đặc
Ag + 2HNO3 -> AgNO3 + NO2 + H2O
Cu + 4HNO3 -> Cu(NO3)2 +2NO2 + 2H2O
-> nNO2=nAg + 2nCu=0,02+0,03.2=0,08 mol -> V NO2=0,08.22,4=1,792 lít
a)
-Cho vào H2O :
+ tan : AgNO3
+ko tan :AgCl
b) - Dùng nam châm hút sắt
_ 2 chất còn lại cho vào nước
+ Tan : AgNO3
+ ko tan :Cu
c) - cho tàn đóm đỏ vào 3 khí , khí duy trì sự cháy là O2
- khí mùi hắc ,màu vàng lục là Cl2
-khí ko màu ,ko mùi, ko duy trì sự cháy : CO2
a) Cho mẫu thử mỗi chất vào ống nghiệm chứa nước. Chất nào tan trong nước là AgNO3, chất nào không tan là AgCl.
b) Dùng nam châm hơ qua mỗi chất. Chất nào bị nam châm hút là Fe. Cho mẫu thử Cu và AgNO3 vào mỗi ống nghiệm chứa nước. Mẫu nào tan được là AgNO3, không tan là Cu.
c) Đưa que đốm còn tàn đỏ qua từng khí. Trường hợp làm que đốm cháy sáng là khí O2. Trường hợp khí có mùi hắc và màu vàng lục là Cl2. Trường hợp làm que đốm tắt đó là CO2.