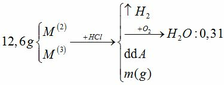
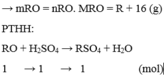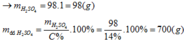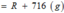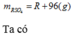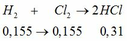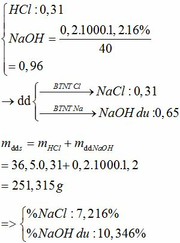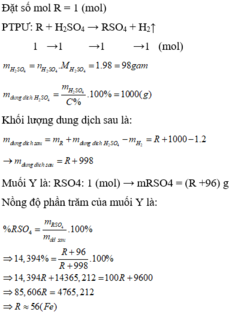1.hòa tan hoàn toàn 16 gam oxit của kim loại M hóa trị II trong dung dịch H2SO4 14,7% vừa đủ , sau phản ứng thu được dung dịch A có nồng độ 18,52%.Đun từ từ dung dịch A cho bay hơi hết , còn lại 56,2 gam muối khan
2.cần phải lấy bao nhiêu gam naoh và bao nhiêu lit dung dịch NaOH 0,4M để pha chế 2 lit dung dịch NaOH 2M (D=1,05g/ml) , biết DH2O=1g/ml
help me !cần gấp