Một hỗn hợp khí A gồm CO, CO2. Trộn A với không khí theo tỉ lệ thể tích 1:4. Sau khi đốt cháy hết khí CO thì hàm lượng phần trăm thể tích của N2 trong hỗn hợp mới thu được tăng 3,36% so với hỗn hợp trước phản ứng. Tính phần trăm thể tích của hai khí trong hỗn hợp A. Giả thiết không khí chỉ có N2, O2 trong đó O2 chiếm 1/5 thể tích không khí.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Không mất tính tổng quát, giả sử trộn 1 mol A với 4 mol không khí.
\(n_{N_2}=4.80\%=3,2mol\\ n_{O_2}=0,8mol\\ \%n_{N_2\left(bđ\right)}=\dfrac{3,2}{5}.100\%=64\%\\ n_{hhsau}=\dfrac{3,2}{64\%+3,36\%}=\dfrac{2000}{421}\left(mol\right)\\ CO+\dfrac{1}{2}O_2-^{t^0}>CO_2\\ n_{CO}=a;n_{CO_2}=b\left(mol\right)\\ a+b=1\\ a+b+3,2+0,8-\dfrac{1}{2}a=\dfrac{2000}{421}\\ a=\dfrac{210}{421};b=\dfrac{211}{421}\\ \%V_{CO}=\dfrac{\dfrac{210}{421}}{\dfrac{2000}{421}}=10,5\%\\ \%V_{CO_2}=89,5\%\)

Đáp án:
%VCO=VCO= 49,88%
%VCO2=VCO2= 50,12%
Giải thích các bước giải:
Giả sử hỗn hợp AA có thể tích là 1l1l
→Vkk=4(l)→Vkk=4(l)
mà %VN2VN2 chiếm 80% VkkVkk
→VN2=4∗80:100=3,2(l)→VN2=4∗80:100=3,2(l)
→→ %VN2VN2 trong hỗn hợp ban đầu là: %VN2=VN2=3,253,25 * 100%
Gọi xx thể tích của COCO trong AA (x>0)(x>0)
Phương trình đốt cháy:
2CO+O2t∘→2CO22CO+O2→t∘2CO2
( mol ) x →→ 0,5x
VhhVhh sau khi đốt cháy là: Vhh=5−0,5x(l)Vhh=5−0,5x(l)
→→ %VN2=VN2=3,25−0,5x∗1003,25−0,5x∗100%
Sau phản ứng cháy %VN2VN2 tăng 3,36%
→→ 3,25−0,5x−3,25−0,5x− 3,25=3,363,25=3,36%
→x=0,4988(l)→x=0,4988(l)
→→ %VCOVCO trong A = 49,88%
→→ %VCO2VCO2 trong A = 100% - 48,88 = 50,12%

Gọi thể tích của CO và CO2 trong hh A là x và y lít
=> thể tích không khí trộn với A là: 4(x+y)
Tổng thể tích của hh trộn: V = 5(x+y)
trong đó: V O2 = \(\dfrac{4\left(x+y\right)}{5}\)và V N2 = \(\dfrac{16\left(x+y\right)}{5}\)
Ban đầu thì
%V N2 = \(\dfrac{16\left(x+y\right)}{5}\) : 5(x+y) = 64%
2CO + O2 to→ 2CO2
x x/2 x
Tổng thể tích hh sau khi đốt = V CO2 (có sẵn và sinh ra từ pư) + V O2 còn lại + V N2 (không đổi)
V' = x+y + \(\dfrac{16\left(x+y\right)}{5}\) + \(\dfrac{4\left(x+y\right)}{5}\) - \(\dfrac{x}{2}\) = 5(x+y) - \(\dfrac{x}{2}\)
%V N2 sau pư = \(\dfrac{16\left(x+y\right)}{5}\): \(5\left(x+y\right)-\dfrac{x}{2}\) = 64% + 3,36% = 67,36 %
=> 16(x+y) = \(0,6736.\left(25\left(x+y\right)-\dfrac{5x}{2}\right)\)
<=> 0,84(x+y) = 1,684 x
=> \(\dfrac{x}{x+y}\) =\(\dfrac{0,084}{1,684}\)≈ 49,88%
=> %V CO = %V CO2 = 50%

Gọi thể tích của CO và CO2 trong hh A là x và y lít
=> thể tích không khí trộn với A là: 4(x+y)
Tổng thể tích của hh trộn: V = 5(x+y)
trong đó: V O2 = 4(x+y)/5 và V N2 = 16(x+y)/5
Ban đầu thì
%V N2 = 16(x+y)/5 : 5(x+y) = 64%
Phản ứng đốt:
2CO + O2 → 2CO2
x x/2 x
Tổng thể tích hh sau khi đốt = V CO2 (có sẵn và sinh ra từ pư) + V O2 còn lại + V N2 (không đổi)
V' = x+y + 16(x+y)/5 + 4(x+y)/5 - x/2 = 5(x+y) - x/2
%V N2 sau pư = 16(x+y)/5 : [5(x+y) - x/2] = 64% + 3,36% = 67,36 %
=> 16(x+y) = 0,6736 . [25(x+y) -5x/2]
<=> 0,84(x+y) = 1,684 x
=> x/(x+y) = 0,084/1,684 ≈ 49,88%
=> %V CO = %V CO2 = 50%

Gọi thể tích CO và CO2 lần lượt là x và y (ml)
Tổng thể tích hỗn hợp trộn là:
V = VX + Vkk = 50 + 200 = 250 (ml)
VO2 = 20% . 200 = 40 (ml)
=> VN2 = 200 - 40 = 160 (ml)
%VN2 bđ = VN2 / V . 100% = 160/250 . 100% = 64%
PTPƯ:
2CO + O2 --to--> 2CO2
x ---------> x/2 ---------> x
Tổng thể tích hỗn hợp sau PƯ:
V’ = VCO2 (ban đầu + sau pư) + VO2 còn lại + VN2 (không đổi)
= (x + y) + (40 - x/2) + 160 = 200 + x/2 + y (ml)
%VN2 sau pư = 160/(200 + x/2 + y) . 100% = 64% + 3,36% = 67,36%
Ta có hpt:
x + y = 50;
160/(200 + x/2 + y) . 100% = 67,36%
=> x ≈ 25 (ml)
=> %VCO = 25/50 . 100% = 50%

Đáp án : A
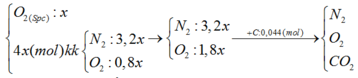
C + O2 à CO2 ( số mol khí trước và sau phản ứng không đổi)
=> nCO2 = nC = 0,044 = 5x.22% => x = 0,04 mol
m = mY + mO2 = mKCl. 100 19 , 893 + 32.0,04 = 8,77g

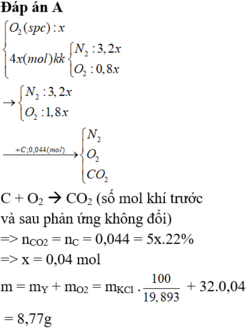
Gọi thể tích của CO và CO2 trong hh A là x và y lít
=> thể tích không khí trộn với A là: 4(x+y)
Tổng thể tích của hh trộn: V = 5(x+y)
trong đó: V O2 = 4(x+y)/5 và V N2 = 16(x+y)/5
Ban đầu thì
%V N2 = 16(x+y)/5 : 5(x+y) = 64%
Phản ứng đốt:
2CO + O2 → 2CO2
x x/2 x
Tổng thể tích hh sau khi đốt = V CO2 (có sẵn và sinh ra từ pư) + V O2 còn lại + V N2 (không đổi)
V' = x+y + 16(x+y)/5 + 4(x+y)/5 - x/2 = 5(x+y) - x/2
%V N2 sau pư = 16(x+y)/5 : [5(x+y) - x/2] = 64% + 3,36% = 67,36 %
=> 16(x+y) = 0,6736 . [25(x+y) -5x/2]
<=> 0,84(x+y) = 1,684 x
=> x/(x+y) = 0,084/1,684 ≈ 1/2 = 50%
=> %V CO = %V CO2 = 50%
G/s có 1l hỗn hợp