Giúp mik bài này với Bài tập 2: Cho thí nghiệm cốc 1: đồ nước mưa, cốc 2 hòa hỗn hợp urê và kali vào lượng nước bằng cốc 1 rồi đặt 2 cây còn nguyên rễ thuộc cùng 1 loài, cùng giai đoạn sinh trường vào cốc sao cho chỉ có rễ ngập trong nước. Yêu cầu: 1. Môi trường trong các cốc thí nghiệm là loại môi trường nào? Ở mỗi môi trường đó, nước và chất tan xâm nhập vào tế bào lông hút bằng con đường nào? 2. Dòng nước và ion khoáng sau khi được hấp thụ vàolông hút được vận chuyển vào mạch gỗ của rễ bằng những con đường nào? Sự khác nhau giữa các con đường đó? 3. Mô tả hiện tưrợng sau 1 tuần thực hiện thínghiệm? 4. Trong thínghiệm trên, cung cấp đủ phân bón nhưng không có nước tốc độ lớn của cây có sự thay đổi như thế nào? Kết luận được rút ra từ tình huống này là gì?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
Giả sử dùng a (mol) Na
TN1:
PTHH: 2Na + 2H2O --> 2NaOH + H2
a------>a--------->a
=> mNaOH = 40a (g)
TN2:
PTHH: 2Na + 2C2H5OH --> 2C2H5ONa + H2
a--------->a---------------->a
=> mC2H5ONa = 68a (g)
=> 68a - 40a = 14
=> a = 0,5 (mol)
=> mNa = 0,5.23 = 11,5 (g)
b)
\(\left\{{}\begin{matrix}m_{H_2O}=0,5.18=9\left(g\right)\Rightarrow V_{H_2O}=\dfrac{9}{1}=9\left(ml\right)\\m_{C_2H_5OH}=0,5.46=23\left(g\right)\Rightarrow V_{C_2H_5OH}=\dfrac{23}{0,8}=28,75\left(ml\right)\end{matrix}\right.\)
=> Độ rượu = \(\dfrac{28,75}{28,75+9}.100=76,159^o\)

Mỗi phần, $m_{muối} = 8,1 : 3 = 2,7(gam)$
Giả sử : Kết tủa phần 1 chỉ có AgCl
Phần 1 :
$RCl_2 + 2AgNO_3 \to R(NO_3)_2 + 2AgCl$
$n_{AgCl} = \dfrac{5,74}{143,5} = 0,04(mol)$
$n_{RCl_2} = \dfrac{1}{2}n_{AgCl} = 0,02(mol)$
$\Rightarrow M_{RCl_2} = R+ 71 = \dfrac{2,7}{0,02} = 135$
$\Rightarrow R = 64(Cu)$
Phần 2 :
$n_{CuO} = n_{CuCl_2} = 0,02(mol)$
$\Rightarrow m_{CuO} = 0,02.80 = 1,6(gam) \to$ Giả thiết đúng.
Phần 3 :
$CuCl_2 + B \to BCl_2 + Cu$
Ta có :
$n_{Cu} = n_B = n_{CuCl_2} = 0,02(mol)$
Suy ra:
$0,02(64 - B) = 0,16 \Rightarrow B = 56(Fe)$

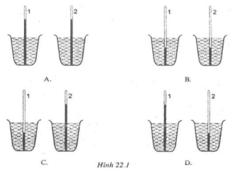
Chọn D
Vì khi đặt nhiệt kế 1 vào cốc đựng nước nóng thì độ chỉ của nhiệt kế sẽ cao hơn so với nhiệt kế 2 đựng vào cốc nước lạnh.

MgO không tan trong nước.
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\\ m_{tăng}=m_{CaO}=5,6\left(g\right)\\ \Rightarrow m_{MgO}=8-5,6=2,4\left(g\right)\)

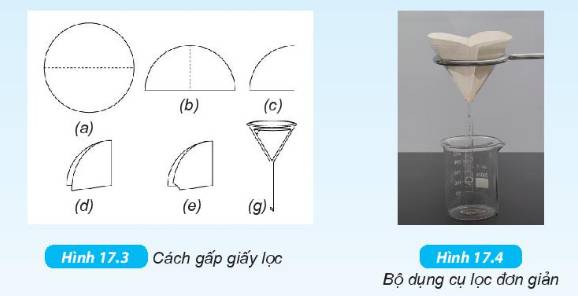
Màu sắc nước gạn và nước lọc khác nhau. Nước gạn có màu nâu đục, còn nước lọc trong suốt do đã lọc được lớp đất bẩn đi.

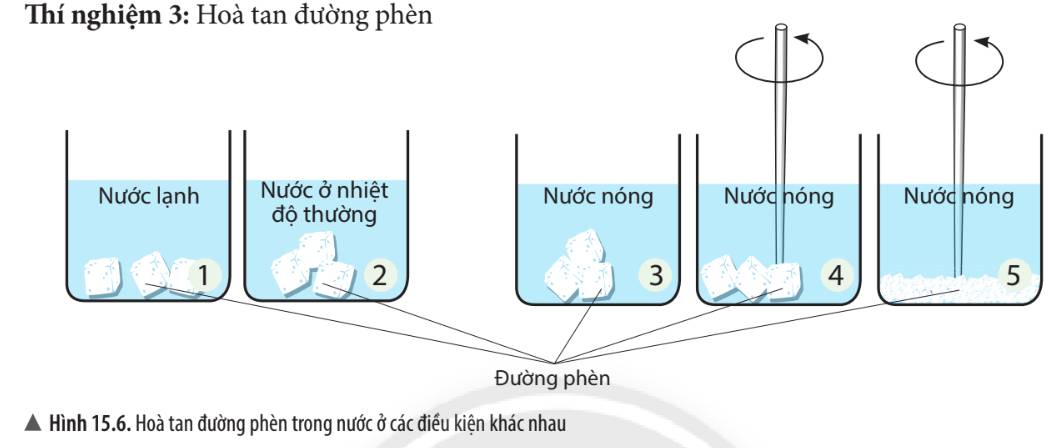
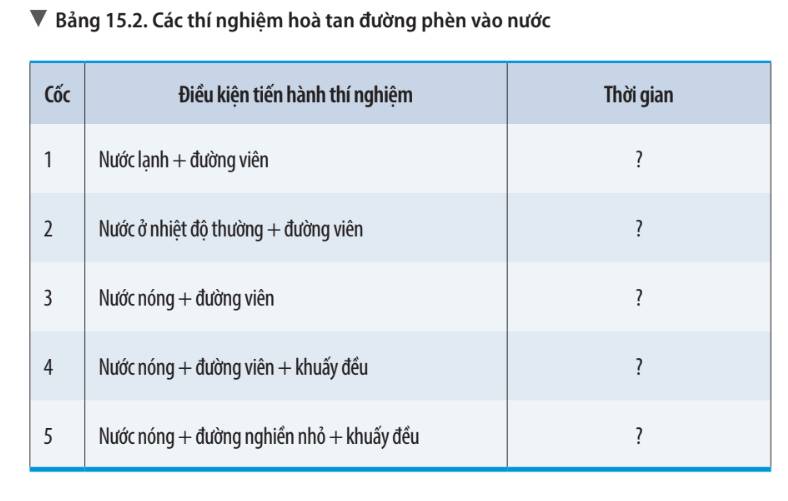
- Đường ở cốc nước số 1 tan chậm nhất. Đường ở cốc nước số 5 tan nhanh nhất
- Giải thích:
+ Đường ở cốc nước số 1 tan chậm nhất vì cốc số 1 là cốc nước lạnh, viên đường to và không được khuấy đều. trong nước lạnh các phân tử nước chuyển động chậm, đồng thời các phân tử đường to và không được khuấy đều nên các phân tử đường khó khăn xen vào giữa các phân tử nước nhanh chóng. Vậy nên mất thời gian lâu nhất
+ Đường ở cốc nước số 5 tan nhanh nhất vì ở cốc nước số 5 là cốc nước nóng, các viên đường đã được nghiền nhỏ và được khuấy đều. Vậy nên chuyển động giữa các phân tử nước và đường sẽ nhanh chóng xen vào nhau tạo ra hỗn hợp đồng nhất chỉ trong một thời gian ngắn

- Pư xong, trong 2 cốc chỉ thu được dd trong suốt
→ CaCO3 và 2 kim loại A, B tan hết.
Ta có: nCaCO3 = 0,1 (mol) = nCO2
⇒ m cốc 1 tăng = mCaCO3 - mCO2 = 10 - 0,1.44 = 5,6 (g)
Mà: Sau pư khối lượng 2 cốc bằng nhau.
⇒ m cốc 2 tăng = 5,6 (g) = 5,8 - mH2
⇒ mH2 = 0,2 (g) ⇒ nH2 = 0,1 (mol)
Vì: A và B đều thuộc nhóm IA → gọi chung là X.
PT: \(2\overline{X}+2H_2O\rightarrow2\overline{X}OH+H_2\)
Theo PT: \(n_{\overline{X}}=2n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow M_{\overline{X}}=\dfrac{5,8}{0,2}=29\left(g/mol\right)\)
Mà: A và B nằm ở 2 chu kỳ liên tiếp.
⇒ A và B là: Na và K.