Khử hết 3,48 gam một oxit của kim loại R cần 1,344 lit \(H_2\) (đktc). Tìm công thức oxit.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi CT của oxit là R2On(n là hóa trị của R)
có : nH2=1,344/22,4=0,06(mol)
R2On+nH2→2R+nH2O
Theo phương trình trên , ta có :
nR2On=1/n.nH2=0,06/n(mol)
⇒mR2On=0,06/n.(2R+16n)=3,48(gam)
⇒R=21n
Nếu n=1 thì R=21(loại)
Nếu n=2nthì R=42(loại)
Nếu n=3thì R=63(loại)
Nếu n=8/3 thì R=56(Fe)
Ta có Fe:O=2:8/3=3:4
Vậy CT của oxit cần tìm là Fe3O4
Gọi x là hóa trị của R
Gọi CTHH của R là R2On
Ta có: nH2= 1,344/22,4= 0,06(mol)
PTHH: R2On + nH2 → 2R + nH2O.
Theo PT trên, ta có: R/n = 21.
- Nếu n = 1 thì R = 21 (loại)
- Nếu n = 2 thì R = 42 (loại)
- Nếu n = 3 thì R = 63 (loại)
- Nếu n = 8/3 thì R = 56 (TM) (Fe)
Ta có: \(\dfrac{Fe}{O}\)=\(\dfrac{2}{\dfrac{8}{3}}\) = \(\dfrac{3}{4}\)
=> CTHH của oxit cần tìm là Fe3O4


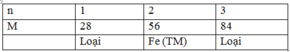
Ta có bảng sau:
n |
1 |
2 |
3 |
4 |
M |
21 (loại) |
42 (loại) |
63 (loại) |
84 (loại) |
=> loại trường hợp này


CTHH: AxOy
\(n_{H_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
PTHH: AxOy + yH2 --to--> xA + yH2O
\(\dfrac{0,06}{y}\)<--0,06---->\(\dfrac{0,06x}{y}\)
2A + 2nHCl --> 2ACln + nH2
\(\dfrac{0,06x}{y}\)---------------->\(\dfrac{0,03xn}{y}\)
=> \(\dfrac{0,03xn}{y}=\dfrac{1,008}{22,4}=0,045\left(mol\right)\)
=> \(\dfrac{y}{x}=\dfrac{2}{3}n\)
\(M_{A_xO_y}=\dfrac{3,48}{\dfrac{0,06}{y}}=58y\left(g/mol\right)\)
=> \(x.M_A=42y\)
=> \(M_A=\dfrac{42y}{x}=28n\left(g/mol\right)\)
Xét n = 2 thỏa mãn => MA = 56 (g/mol)
=> A là Fe
\(\dfrac{x}{y}=\dfrac{3}{2n}=\dfrac{3}{4}\) => CTHH: Fe3O4

Đặt a là hoá trị kim loại M cần tìm (a: nguyên, dương)
\(M_2O_a+aH_2\rightarrow\left(t^o\right)2M+aH_2O\left(1\right)\\ 2M+2aHCl\rightarrow2MCl_a+aH_2\left(2\right)\\Ta.có:n_{H_2\left(2\right)}=\dfrac{1,008}{22,4}=0,045\left(mol\right)\\ n_{H_2\left(1\right)}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\\ \Rightarrow n_{O\left(trong.oxit\right)}=n_{H_2O}=n_{H_2\left(1\right)}=0,06\left(mol\right)\\ \Rightarrow m_M=3,48-0,06.16=2,52\left(g\right)\\ n_{H_2\left(2\right)}=0,045\left(mol\right)\\ \Rightarrow n_{M\left(2\right)}=\dfrac{0,045.2}{a}=\dfrac{0,09}{a}\left(mol\right)\\ \Rightarrow M_M=\dfrac{2,52}{\dfrac{0,09}{a}}=28a\left(\dfrac{g}{mol}\right)\)
Xét các TH: a=1; a=2; a=3; a=8/3 thấy a=2 thoả mãn khi đó MM=56(g/mol), tức M là Sắt (Fe=56)
Đặt CTTQ của oxit sắt cần tìm là FemOn (m,n: nguyên, dương)
\(n_{Fe}=\dfrac{2,52}{56}=0,045\left(mol\right)\\n_O=0,06\left(mol\right)\)
=> m:n= 0,045:0,06=3:4
=>m=3;n=4
=> CTHH oxit: Fe3O4 (Sắt từ oxit)
-Em chỉ mới lập được phương trình hóa học tổng quát thôi, em chưa tính được.

Gọi CT oxit là M2Om
Mol H2 TN1=0,06 mol
Mol H2 TN2=0,045 mol
M2Om + mH2→ 2M + mH2O
0,06/m mol<=0,06 mol. =>0,12/m mol
=>0,06(2M+16m)/m=3,48
2M + 2nHCl→ 2MCln + nH2
0,12/m mol. 0,045 mol
⇒⇒0,045.2/n=0,12/m⇒⇒m=8/3; n=2 tm
Thay m=8/3 vào công thức tính m có M=56 FeFe
Oxit là Fe3O4 vì n=8/3

Xét phương trình: \(M_xO_y+H_2\rightarrow M+H_2O\)
Bảo toàn khối lượng và \(H_2\) ta có:
\(n_{H_2O}=n_{H_2}=0,06\)
\(\Rightarrow m_M=3,46+0,06.2-0,06.18=2,52\left(g\right)\)
Khi cho M phản ứng với HCl ta có \(n_{H_2}=0,045\)
Xét M chỉ có hóa trị 2,3 nên dễ thấy với hóa trị 2 thì:
\(n_M=n_{H_2}=0,045\Rightarrow M=\frac{2,52}{0,045}=56=Fe\)
Ta có \(\frac{n_M}{n_O}=\frac{0,045}{0,06}=\frac{3}{4}\)
\(\Rightarrow\) CT của oxit là: \(Fe_3O_4\)



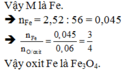
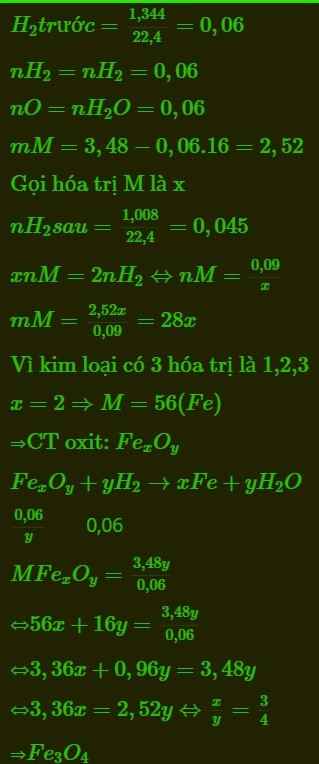

Gọi x là hóa trị của R
Gọi CTHH của R là R2On
Ta có: nH2= 1,344/22,4= 0,06(mol)
PTHH: R2On + nH2 → 2R + nH2O.
Theo PT trên, ta có: R/n = 21.
- Nếu n = 1 thì R = 21 (loại)
- Nếu n = 2 thì R = 42 (loại)
- Nếu n = 3 thì R = 63 (loại)
- Nếu n = 8/3 thì R = 56 (TM) (Fe)
Ta có: Fe/O=2/8/3 = 3/4
=> CTHH của oxit cần tìm là Fe3O4