Anion X- và cation Y+ có cấu hình e giống nhau. Phát biểu nào sau đây đúng:
A. Nguyên tố X và Y thuộc cùng chu kỳ trong bảng hệ thống tuần hoàn.
B. Số e trong lớp vỏ nguyên tử của Y nhiều hơn trong lớp vỏ nguyên tử của X là 2e
C. Số e trong lớp ngoài cùng của ngtử Y nhiều hơn trong lớp vỏ e ngoài cùng của ngtử X là 2e
D. Số proton trong ngtử X nhiều hơn trong Y là 1 hạt

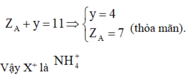
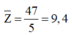
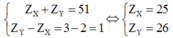
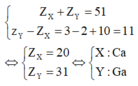
C