Để khử hoàn toàn 3,04 gam hỗn hợp X gồm FeO, Fe 2 O 3 , Fe 3 O 4 thì cần 0,05 mol H 2 . Mặt
khác hòa tan hoàn toàn 3,04 gam hỗn hợp X trong dung dịch H 2 SO 4 đặc nóng thì thu được khí SO2 là sản phẩm khử duy nhất. Tính thể tích khí SO2(đktc)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Quy đổi hỗn hợp X về hỗn hợp hai chất FeO và Fe2O3 với số mol là x, y
Ta có:
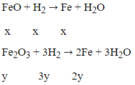
Có: x + 3y = 0,05 và 72x +160y = 3,04
⇒ x = 0,02mol; y = 0,01mol

Vậy VSO2 = 0,01 . 22,4 = 0,224 lít hay 224ml

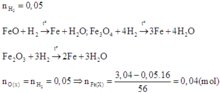
Coi hỗn hợp X ban đầu gồm Fe và O.
Khi đó áp dụng định luật bảo toàn mol electron, ta có:
![]()
Đáp án A.

đề là 0,05 h2..mới đúng ..có h2..thì tìm đk o-..rồi bảo toàn e là ra

hỗn hợp X( quy đổi) ----> Fe( x mol) ,O( y mol)
Cho X+ H2:
Bảo toàn khối lượng: m(hh X)= m(Fe)+m(O)= 56x+16y=3,04
Bảo toàn H: n(H2O)=n(H2)=0,05 Bảo toàn O: n(O)=n(H2O)=0,05=y suy ra x=0,04
Cho X+H2SO4: ----> SO2 a mol
Fe--->Fe(3+) +3e 2O+ 4e---> 2O(2-)
0,04 3.0,04 0.05 2.0,05
S(+6)+ 2e----> S(+4)
2a a
Bảo toàn e: 3.0,04= 2.0,05+2a suy ra a=0.01 suy ra V=0,224 l

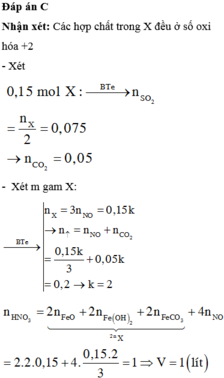
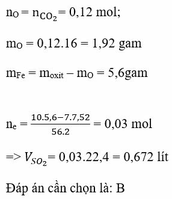
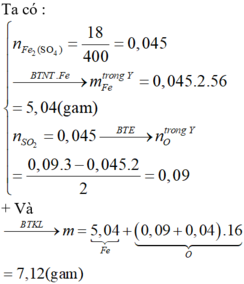
Viết lại hỗn hợp X gồm: \(FeO,Fe_2O_3\)
Gọi số mol của FeO và Fe2O3 lần lược là x, y.
\(FeO\left(a\right)+H_2\left(a\right)\rightarrow Fe+H_2O\)
\(Fe_2O_3\left(b\right)+3H_2\left(3b\right)\rightarrow2Fe+3H_2O\)
\(2FeO\left(a\right)+4H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+SO_2\left(\dfrac{a}{2}\right)+4H_2O\)
Ta có hệ: \(\left\{{}\begin{matrix}72a+160b=3,04\\a+3b=0,05\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}a=0,02\\b=0,01\end{matrix}\right.\)
\(\Rightarrow n_{SO_2}=\dfrac{a}{2}=\dfrac{0,02}{2}=0,01\left(mol\right)\)
\(\Rightarrow V_{SO_2}=0,01.22,4=0,224\left(l\right)\)
Còn Fe3O4 trong hh X nữa mà