Khử hết 3,48 gam một oxit của kim loại R cần 1,344 lit H2 (đktc). Tìm công thức oxit.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi x là hóa trị của R
Gọi CTHH của R là R2On
Ta có: nH2= 1,344/22,4= 0,06(mol)
PTHH: R2On + nH2 → 2R + nH2O.
Theo PT trên, ta có: R/n = 21.
- Nếu n = 1 thì R = 21 (loại)
- Nếu n = 2 thì R = 42 (loại)
- Nếu n = 3 thì R = 63 (loại)
- Nếu n = 8/3 thì R = 56 (TM) (Fe)
Ta có: Fe/O=2/8/3 = 3/4
=> CTHH của oxit cần tìm là Fe3O4


Ta có bảng sau:
n |
1 |
2 |
3 |
4 |
M |
21 (loại) |
42 (loại) |
63 (loại) |
84 (loại) |
=> loại trường hợp này


Đặt a là hoá trị kim loại M cần tìm (a: nguyên, dương)
\(M_2O_a+aH_2\rightarrow\left(t^o\right)2M+aH_2O\left(1\right)\\ 2M+2aHCl\rightarrow2MCl_a+aH_2\left(2\right)\\Ta.có:n_{H_2\left(2\right)}=\dfrac{1,008}{22,4}=0,045\left(mol\right)\\ n_{H_2\left(1\right)}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\\ \Rightarrow n_{O\left(trong.oxit\right)}=n_{H_2O}=n_{H_2\left(1\right)}=0,06\left(mol\right)\\ \Rightarrow m_M=3,48-0,06.16=2,52\left(g\right)\\ n_{H_2\left(2\right)}=0,045\left(mol\right)\\ \Rightarrow n_{M\left(2\right)}=\dfrac{0,045.2}{a}=\dfrac{0,09}{a}\left(mol\right)\\ \Rightarrow M_M=\dfrac{2,52}{\dfrac{0,09}{a}}=28a\left(\dfrac{g}{mol}\right)\)
Xét các TH: a=1; a=2; a=3; a=8/3 thấy a=2 thoả mãn khi đó MM=56(g/mol), tức M là Sắt (Fe=56)
Đặt CTTQ của oxit sắt cần tìm là FemOn (m,n: nguyên, dương)
\(n_{Fe}=\dfrac{2,52}{56}=0,045\left(mol\right)\\n_O=0,06\left(mol\right)\)
=> m:n= 0,045:0,06=3:4
=>m=3;n=4
=> CTHH oxit: Fe3O4 (Sắt từ oxit)
-Em chỉ mới lập được phương trình hóa học tổng quát thôi, em chưa tính được.

Gọi CT oxit là M2Om
Mol H2 TN1=0,06 mol
Mol H2 TN2=0,045 mol
M2Om + mH2→ 2M + mH2O
0,06/m mol<=0,06 mol. =>0,12/m mol
=>0,06(2M+16m)/m=3,48
2M + 2nHCl→ 2MCln + nH2
0,12/m mol. 0,045 mol
⇒⇒0,045.2/n=0,12/m⇒⇒m=8/3; n=2 tm
Thay m=8/3 vào công thức tính m có M=56 FeFe
Oxit là Fe3O4 vì n=8/3

CTHH: AxOy
\(n_{H_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
PTHH: AxOy + yH2 --to--> xA + yH2O
\(\dfrac{0,06}{y}\)<--0,06---->\(\dfrac{0,06x}{y}\)
2A + 2nHCl --> 2ACln + nH2
\(\dfrac{0,06x}{y}\)---------------->\(\dfrac{0,03xn}{y}\)
=> \(\dfrac{0,03xn}{y}=\dfrac{1,008}{22,4}=0,045\left(mol\right)\)
=> \(\dfrac{y}{x}=\dfrac{2}{3}n\)
\(M_{A_xO_y}=\dfrac{3,48}{\dfrac{0,06}{y}}=58y\left(g/mol\right)\)
=> \(x.M_A=42y\)
=> \(M_A=\dfrac{42y}{x}=28n\left(g/mol\right)\)
Xét n = 2 thỏa mãn => MA = 56 (g/mol)
=> A là Fe
\(\dfrac{x}{y}=\dfrac{3}{2n}=\dfrac{3}{4}\) => CTHH: Fe3O4

Đáp án A
Oxit chưa biết của kim loại nào → Gọi MxOy
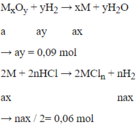
Mà : 56ax + 16ay = 4,8
→ ax = 0,06
→ x : y = ax : ay = 0,06 : 0,09 = 2 : 3 => M2O3
→ n = 0,12 : 0,06 = 2 => M hóa trị II
→ Chỉ có Fe thỏa mãn vì nó có hai hóa trị
Lưu ý: Bài toán này dễ nhầm lẫn nếu không để ý sự thay đổi hóa trị ở 2 phương trình.



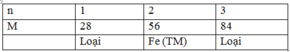
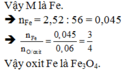
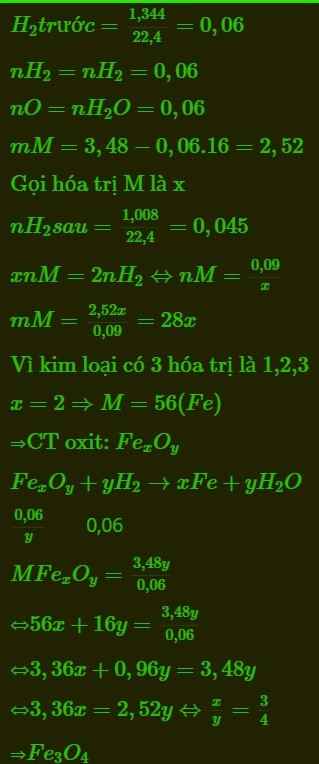
Gọi CT của oxit là R2On(n là hóa trị của R)
có : nH2=1,344/22,4=0,06(mol)
R2On+nH2→2R+nH2O
Theo phương trình trên , ta có :
nR2On=1/n.nH2=0,06/n(mol)
⇒mR2On=0,06/n.(2R+16n)=3,48(gam)
⇒R=21n
Nếu n=1 thì R=21(loại)
Nếu n=2nthì R=42(loại)
Nếu n=3thì R=63(loại)
Nếu n=8/3 thì R=56(Fe)
Ta có Fe:O=2:8/3=3:4
Vậy CT của oxit cần tìm là Fe3O4
Gọi x là hóa trị của R
Gọi CTHH của R là R2On
Ta có: nH2= 1,344/22,4= 0,06(mol)
PTHH: R2On + nH2 → 2R + nH2O.
Theo PT trên, ta có: R/n = 21.
- Nếu n = 1 thì R = 21 (loại)
- Nếu n = 2 thì R = 42 (loại)
- Nếu n = 3 thì R = 63 (loại)
- Nếu n = 8/3 thì R = 56 (TM) (Fe)
Ta có: \(\dfrac{Fe}{O}\)=\(\dfrac{2}{\dfrac{8}{3}}\) = \(\dfrac{3}{4}\)
=> CTHH của oxit cần tìm là Fe3O4