Để đốt cháy hoàn toàn 5,4 gam kim loại R chỉ cần dùng 90% lượng oxi sinh ra khi
phân hủy 39,5gam KMnO 4 . Hãy xác định kim loại R.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

n_KMnO4 = 5,53 : 158 = 0,035 (mol)
Ta có ptpu
2KMnO4→ K2MnO4+MnO2+O22KMnO4→ K2MnO4+MnO2+O2 (nhiệt độ )
0,035---------------------------------------0,0175 (mol)
DO lượng Oxi cần dùng là 80%
\Rightarrow n_O2 = 0,014 (mol)
Gọi Khối lượng mol của R là A (gam) , hóa trị của R là n
\Rightarrow n_R = 0,672/A
Ta có phản ứng
4R+nO2→ 2R2On4R+nO2→ 2R2On (nhiệt độ )
0,672/A...0,014..........................(mol)
\Rightarrow 0,672/A . n = 0,014 .4
\Rightarrow 0,672 . n = 0,056A
n là hóa trị của kim loại \Rightarrow n chỉ có thể = 1,2,3,4
Bạn lập bảng thử chọn
\Rightarrow n = 2 \Rightarrow A = 24
Vậy kim loại R là Magie : Mg

a)\(n_{KMnO_4}\)=39,5:158=0,25(mol)
Ta có PTHH:
2\(KMnO_4\)\(\underrightarrow{to}\)\(K_2MnO_4+MnO_2+O_2\)(1)
......0,25..............................................0,125(mol)
Theo PTHH:\(n_{O_2\left(1\right)}\)=0,125(mol)
=>\(n_{O_2\left(cần\right)}\)=90%.0,125=0,1125(mol)
=>\(m_{O_2\left(cần\right)}\)=0,1125.32=3,6(g)
Gọi n là hóa trị của R
4R+n\(O_2\)\(\underrightarrow{to}\)2\(R_2O_n\)
4R...32n..................(g)
5,4....3,6..................(g)
Theo PTHH:3,6.4R=5,4.32n=>R=12n
Vì n là hóa trị của R nên n\(\in\){1;2;3;\(\dfrac83\)}
Biện luận:
| n | 1 | 2 | 3 | 8/3 |
| R | 12 | 24 | 36 | 32 |
=>n=2;R=24(Mg) là phù hợp
Vậy R là Mg
b)\(n_{Mg}\)=5,4:24=0,225(mol)
Ta có PTHH:
Mg+2HCl->Mg\(Cl_2\)+\(H_2\)
0,225..0,45........................(mol)
Theo PTHH:\(m_{HCl}\)=0,45.36,5=16,425(g)
mà \(C_{\%ddHCl}\)=14,6%
=>\(m_{dd\left(gt\right)}\)=16,425:14,6%=112,5(g)
mà dd lấy dư 20% nên:
=>\(m_{dd\left(cần\right)}\)=112,5+20%.112,5=135(g)

áp dụng ĐLBTKL:
mR + mO2 = mR2O3
=> mO2=20,4-10,8=9,6(g)
=> nO2=9,6/32=0,3(mol)
4R + 3O2 ---to---> 2R2O3
0,4........0,3
MR=10,8/0,4=27(g)
=> R là nhôm ......Al

Đáp án A
Dựa vào bản chất phản ứng của X với NaHCO 3 , bảo toàn nguyên tố O; bảo toàn electron trong phản ứng đốt cháy X, ta có :
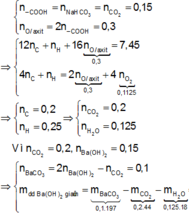
= 8,65 gam

\(2KMnO_4-->MnO_2+K_2MnO_4+O_2\)
0,035___________0,0175___0,0175_____0,0175
\(4R+nO_2-->2R_2O_n\)
0,0175.4/n___0,0175(1)
\(n_{KMnO_4}=\dfrac{5,53}{158}=0,035\left(mol\right)\)
=>\(n_R=\dfrac{0,84}{R}\left(mol\right)\) (2)
từ (1), (2) => \(\dfrac{0,0175.4}{n}=\dfrac{0,84}{R}\)
r thay n theo hóa trị từ 1-> 4 nhớ lập bảng bn nhé
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,035 ------------------------------------- 0,0175
\(4R+xO_2\underrightarrow{t^o}2R_2O_x\)
\(\dfrac{0,07}{x}\) -- 0,0175
\(n_{KMnO_4}=\dfrac{5,53}{158}=0,035\left(mol\right)\)
\(n_{O_2}=\dfrac{1}{2}.0,035=0,0175\left(mol\right)\)
\(n_R=\dfrac{0,84}{R}\left(mol\right)\)
Ta có:
\(\dfrac{0,84}{R}=\) \(\dfrac{0,07}{x}\)\(\Leftrightarrow R=12x\)
Biện luận:
| x | 1 | 2 | 3 |
| R | 12 | 24 | 36 |
Chọn x = 2, R = 24.
Vậy R là Mg.

\(a) 4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3\\ n_{Al} = \dfrac{5,4}{27} = 0,2(mol)\\ n_{Al_2O_3} = \dfrac{1}{2}n_{Al} = 0,1(mol) \Rightarrow m_{Al_2O_3} = 0,1.102 = 10,2(gam)\\ b) n_{O_2} = \dfrac{3}{4}n_{Al} = 0,15(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{KMnO_4} = 2n_{O_2} = 0,3(mol) \Rightarrow m_{KMnO_4} = 0,3.158 = 47,4(gam)\)
a, PT: \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
Theo PT: \(n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=0,1\left(mol\right)\)
\(\Rightarrow m_{Al_2O_3}=0,1.102=10,2\left(g\right)\)
b, Theo PT: \(n_{O_2}=\dfrac{3}{4}n_{Al}=0,15\left(mol\right)\)
PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
Theo PT: \(n_{KMnO_4}=2n_{O_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{KMnO_4}=0,2.158=47,4\left(g\right)\)
Bạn tham khảo nhé!

\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\\a, PTHH:4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\\ b,n_{O_2}=\dfrac{3}{4}.n_{Al}=\dfrac{3.0,2}{4}=0,15\left(mol\right)\\ \Rightarrow V_{O_2\left(đktc\right)}=0,15.22,4=3,36\left(l\right)\\ c,2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\\ n_{KMnO_4}=2.n_{O_2}=2.0,15=0,3\left(mol\right)\\ \Rightarrow m_{KMnO_4}=158.0,3=47,4\left(g\right)\)

Gọi hóa trị kim loại M là x (x€ N*)
PTPƯ:
(1) 4M + xO2 ---> 2M2Ox
số mol kim loại M = m/M
số mol oxit kl là = 1.25m /( 2M+16x)
Theo phương trình (1), ta có:
2. m/M = 4. 1.25m/( 2M+16x)
=> M= 32x
Vì x là hóa trị kim loại nên ta biện luận:
* x=1 -> M=32 ( lưu huỳnh )-> M là phi kim (loại)
* x=2 -> M=64 (đồng)
* x=3 -> M=96 ->loại
Vậy R là Cu.
CTTQ: MxOy
Hóa trị của M: 2y/x
Pt: 2xM + yO2 --to--> 2MxOy
...\(\frac{0,5xm}{32y}\)<-.\(\frac{0,25m}{32}\)
Áp dụng ĐLBTKL, ta có:
mM + mO2 = mMxOy
=> mO2 = mMxOy - mM = 1,25m - m= 0,25m (g)
=> nO2 = \(\frac{0,25m}{32}\) mol
Ta có: m = \(\frac{0,5xm}{32y}\) . MM
<=> 1 = \(\frac{0,5x}{32y}\) . MM
<=> 32y = 0,5x .MM
=> MM = \(\frac{32y}{0,5x}=\frac{2y}{x}.\frac{16}{0,5}= \frac{2y}{x}.32\)
Biện luận:
| 2y/x | 1 | 2 | 3 |
| M | 32 (loại) | 64 (nhận) |
96 (loại) |
Vậy M là Đồng (Cu)

a. Gọi n là hóa trị của kim loại R.
Theo đề: nR = \(\dfrac{16}{R}\left(mol\right),n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Theo đề ta có PTHH:
\(2R+2nHCl\rightarrow2RCl_n+nH_2\)
Số mol: \(\dfrac{16}{R}\) ___________________ \(\dfrac{16.n}{R.2}\)
The phương trình: nR = \(\dfrac{n}{2}n_{H_2}\)= \(\dfrac{16n}{2R}\left(mol\right)\)
Hay: \(\dfrac{16n}{2R}=0,4\left(mol\right)\)\(\Leftrightarrow R=20n\left(g\right)\)
Biện luận R theo n:
* Khi n = 1 \(\Rightarrow\) R = 20 (loại)
* Khi n = 2 \(\Rightarrow\) R = 40 (chọn)
* Khi n = 3 \(\Rightarrow\) R = 60 (loại)
Vậy R là Can xi (Ca).
\(n_{KMnO_4}=\dfrac{39,5}{158}=0,25\left(mol\right)\)
\(2KMnO_4--t^0->K_2MnO_4+MnO_2+O_2\)
0,25........................................................................0,125(mol)
\(m_{90\%O}=\dfrac{0,125.32.90\%}{100\%}=3,6\left(g\right)\)
\(n_{O_2}=\dfrac{3,6}{32}=0,1125\left(mol\right)\)
\(2xR+yO_2\rightarrow2R_xO_y\)
\(\dfrac{0,225x}{y}\) ......0,1125 .......0,225
\(M_R=\dfrac{5,4}{\dfrac{0,225x}{y}}=\dfrac{24y}{x}\left(1\right)\)
Theo định luật bảo toàn khối lượng ta có
\(m_{R_xO_y}=0,225\left(xM_R+16y\right)=5,4+3,6\)
\(\Leftrightarrow\dfrac{24y}{x}.0,225x+3,6y=9\)
\(\Rightarrow y=1\)
\(\Rightarrow x.M_R=24\left(\dfrac{g}{mol}\right)\)
vậy R: Magie
\(n_R=\dfrac{5,4}{M_R}\)
\(n_{KMnO_4}=0,25\left(mol\right)\)
\(2KMnO_4-t^0->MnO_2+K_2MnO_4+O_2\)
\(0,25mol..................................0,125mol\)
Mà khi đốt cháy hoàn toàn 5,4 g kim loại R chỉ cần dùng một lượng 90% lượng oxi sinh ra nên : \(n_{O_2}=90\%.0,125=0,1125\left(mol\right)\)
\(4R+nO_2->2R_2O_n\)
\(\dfrac{0,45}{n}......0,1125\)
\(\dfrac{5,4}{M_R}=\dfrac{0,45}{n}\)
\(1\le n\le3\)
\(n=1=>M_R=12\left(loại\right)\)
\(n=2=M_R=24\left(Mg\right)\)
\(n=3=>M_R=36\left(loại\right)\)
Vậy R là Mg .