cho hỗn hợp gồm 5,6g Fe 7,8g Zn và dd HNO3 loãng dư sau khi phản ứng xảy ra hoàn toàn thu được 3,36 lít NO (SP duy nhất) đktc và dd X chứa m (g) 1 muối . m=?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Coi B gồm : $Fe(x\ mol) ; O(y\ mol) \Rightarrow 56x + 16y = 8,32(1)$
$n_{NO} = \dfrac{2,688}{22,4} = 0,12(mol)$
Bảo toàn electron : $3n_{Fe} = 2n_O + 3n_{NO}$
$\Rightarrow 3x = 2y + 0,12.3(2)$
Từ (1)(2) suy ra x = 0,14 ; y = 0,03
$n_{Fe(NO_3)_3} = n_{Fe} = 0,14(mol)$
$\Rightarrow m = 0,14.242 = 33,88(gam)$

Quy đổi X thành các đơn chất: Cu (x mol); Fe (l,5y mol); O2 (y mol) => 64x + 116y = 61,2 - 2,4 = 58,8
Bảo toàn electron ta có: ne cho = ne nhận
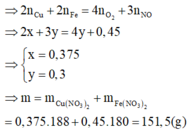
Đáp án B

Coi hh X gồm Fe, Cu và O
Đặt \(n_{Fe\left(Fe_xO_y\right)}=a;n_{Cu}=b;n_{O\left(Fe_xO_y\right)}=c\) ( mol )
\(\Rightarrow m_{hh}=56a+64b+16c=14,64\left(g\right)\) (1)
\(m_{muối}=m_{Fe\left(NO_3\right)_3}+m_{Cu\left(NO_3\right)_2}=242a+188b=47,58\left(g\right)\) (2)
Bảo toàn e: \(3n_{Fe}+2n_{Cu}=2n_O+3n_{NO}=3a+2b=2c+3.0,09\) (3)
\(\left(1\right);\left(2\right);\left(3\right)\Rightarrow\left\{{}\begin{matrix}a=0,15\\b=0,06\\c=0,15\end{matrix}\right.\)
\(\%m_{Cu}=\dfrac{0,06.64}{14,64}.100=26,22\%\)
\(\dfrac{x}{y}=\dfrac{0,15}{0,15}=\dfrac{1}{1}\Rightarrow CTHH:FeO\)

Đáp án A
Gọi x, y lần lượt là số mol Cu va Fe3O4 phản ứng
=>64x + 232y = 61,2 – 2,4 = 58,8 (1)
Sau phản ứng còn 2,4 gam kim loại đó là Cu, nên trong dung dịch có Cu2+, Fe2+
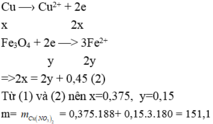

Đáp án : D
Chỉ có Fe phản ứng với HCl
⇒ n H 2 = n F e = 0 , 15 m o l = n F e C l 2
=> m m u ố i = m F e C l 2 = 19,05g

Đáp án : D
Chỉ có Fe + 2HCl à FeCl2 + H2
=> mmuối = m FeCl2 = 127.nFeCl2 = 127.0,15 = 19,05g