Cho 31,25 g nước Clo vào 1 dung dịch có chứa 3,125 g KBr thấy dung dịch chuyển sang màu vàng và KBr vẫn còn dư. Cô cạn dung dịch sau phản ứng thì thu được 2,0125 g rắn khan. Giả sử toàn bộ Clo trong nước Clo đã phản ứng. C% của Clo trong nước Clo là bao nhiêu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(Cl_2+2NaBr\rightarrow2NaCl+Br_2\)
\(n_{Cl_2}=\frac{2,5-1,61}{44,5}=0,02\left(mol\right)\)
\(C\%_{Cl_2}=\frac{0,02.71}{25}.100\%=5,68\%\)
Cl2+2NaBr→2NaCl+Br2
nCl2=2,5−1,6144,5=0,02(mol)
C%Cl2=0,02.7125.100%=5,68%

Gọi số mol Cl2 là a (mol)
PTHH: 2KBr + Cl2 --> 2KCl + Br2
2a<----a------->2a
=> mrắn sau pư = 2,5 - 119.2a + 74,5.2a = 1,61
=> a = 0,01 (mol)
\(C\%_{Cl_2}=\dfrac{0,01.71}{25}.100\%=2,84\%\)
Rắn thu được gồm \(\left\{{}\begin{matrix}KBr\\KCl\end{matrix}\right.\)
mKBr = 2,5 - 0,02.119 = 0,12 (g)
mKCl = 0,02.74,5 = 1,49 (g)

Khi cho 5g Br 2 có lẫn Cl 2 phản ứng với KBr thì khối lượng muối giảm là :
1,600 - 1,155 = 0,445 (g)
Cl 2 + 2KBr → 2KCl + Br 2
Lý thuyết: 71 g 238 g 149 g khối lượng muối giảm đi 238 – 149 = 89 g
Thực tế: x g 0,445 g khối lượng muối giảm
Ta có:
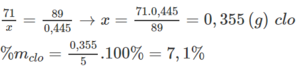

Đáp án B
Đặt
![]()
Khối lượng muối khan giảm là do đã xảy ra phản ứng thay thế các nguyên tử halogen trong muối.
Ta có hệ:
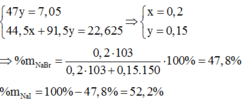

Chọn đáp án C
Gọi số mol của NaBr là x mol; NaI là y mol.
Cho B r 2 vào dung dịch A, chỉ NaI phản ứng.
NaI + 1 2 Br2 → NaBr + 1 2 I2
1 mol NaI → 1 mol NaBr khối lượng giảm 47g
→ n N a I = 7 , 05 47 = 0,15 mol = y
Khi sục khí Clo vào dung dịch A, cả NaBr và NaI phản ứng.
m m u ố i g i ả m = x.(80 – 35,5) + y (127-35,5) = 22,625 g
→ x = 0,2 mol
ð % m N a B r = 0 , 2 . 103 0 , 2 . 103 + 0 , 15 . 150 .100(%) = 47,80(%)

Spu, m giảm= mBr- - mCl-= 1,6-1,155= 0,445 mol
Gọi x là mCl- thì x+0,445 là mBr-
\(Cl_2+2Br^-\rightarrow Br_2+2Cl^-\)
\(\rightarrow n_{Cl^-}=n_{Br^-}\)
\(\Leftrightarrow\frac{x}{35,5}=\frac{x+0,445}{80}\)
\(\Leftrightarrow35m5\left(x+0,445\right)=80x\)
\(\Leftrightarrow x=0,355\)
\(n_{Cl^-}=\frac{0,335}{35,5}\left(mol\right)\)
\(\rightarrow n_{Cl2}=\frac{0,337}{71}\left(mol\right)\)
\(\rightarrow m_{Cl2}=0,335\left(g\right)\)
\(\%_{Cl2}=\frac{0,335.100}{5}=6,7\%\)
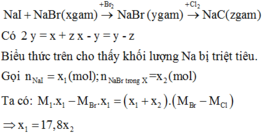
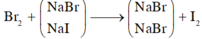
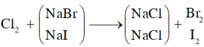
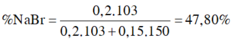
Gọi số mol clo đã phản ứng là x (mol)
PTHH : Cl2 + 2KBr \(\rightarrow\) 2KCl + Br2
x 2x 2x x (mol)
\(\Rightarrow m_{KBr_{dư}}=3,125-2x.\left(80+39\right)=3,125-238x\left(g\right)\)
mrắn khan = \(m_{KBr_{dư}}\)+ mKCl
\(\Leftrightarrow2,0125=3,125-238x+2x.74,5\)\(\Leftrightarrow\) x = 0,0125 (mol)
\(\Rightarrow m_{Cl_2}=0,0125.71=0,8875\left(g\right)\)
\(C\%_{Cl_2}=\dfrac{0,8875}{31,25}.100\%=2,84\%\)