Cho 1 gam axit axetic vào ống nghiệm thứ nhất và 1gam axit fomic vào ống nghiệm thứ hai, sau đó cho vào cả hai ống nghiệm trên một lượng dư bột CaCO3. Đến khi phản ứng xảy ra hoàn toàn thì thể tích khí CO2 thu được (đo ở dùng điều kiện) thoát ra.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Đáp án C
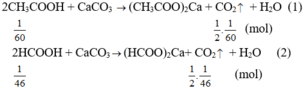
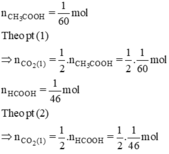
⇒ số mol CO2 thoát ra từ ống nghiệm hai nhiều hơn ống nghiệm thứ nhất.

Đáp án B
Khi nhỏ dung dịch Na2S lần lượt vào 3 ống nghiệm chứa ZnCl2, CuSO4, Pb(NO3)2 thấy cả 3 ống nghiệm đều xuất hiện kết tủa (ZnS, CuS, PbS). Nhỏ tiếp dung dịch HCl dư vào 3 ống nghiệm trên, sau khi phản ứng xảy ra hoàn toàn, các ống nghiệm vẫn còn kết tủa là: (2), (3) do CuS và PbS không tan trong dd HCl còn ZnS tác dụng với HCl tạo thành ZnCl2 và H2S.

Dự đoán Zn ở ống nghiệm 2 (Zn dạng bột) sẽ tan hết trước do diện tích tiếp xúc với dung dịch HCl của Zn dạng bột lớn hơn của Zn dạng hạt.
Zn bột tan hết trước do diện tích tiếp xúc với dd HCl (dư) nhiều hơn -> Tốc độ p.ứ tăng

a)\(n_{Fe}=\dfrac{16,8}{56}=0,3mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,3 0,3 0,3
\(V_{H_2}=0,3\cdot22,4=6,67l\)
\(m_{FeCl_3}=0,3\cdot127=38,1g\)
b)\(n_{Fe_2O_3}=\dfrac{18}{160}=0,1125mol\)
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
0,1125 0,3 0 0
0,1 0,3 0,2 0,3
0,0125 0 0,2 0,3
\(m_{Fe}=0,2\cdot56=11,2g\)
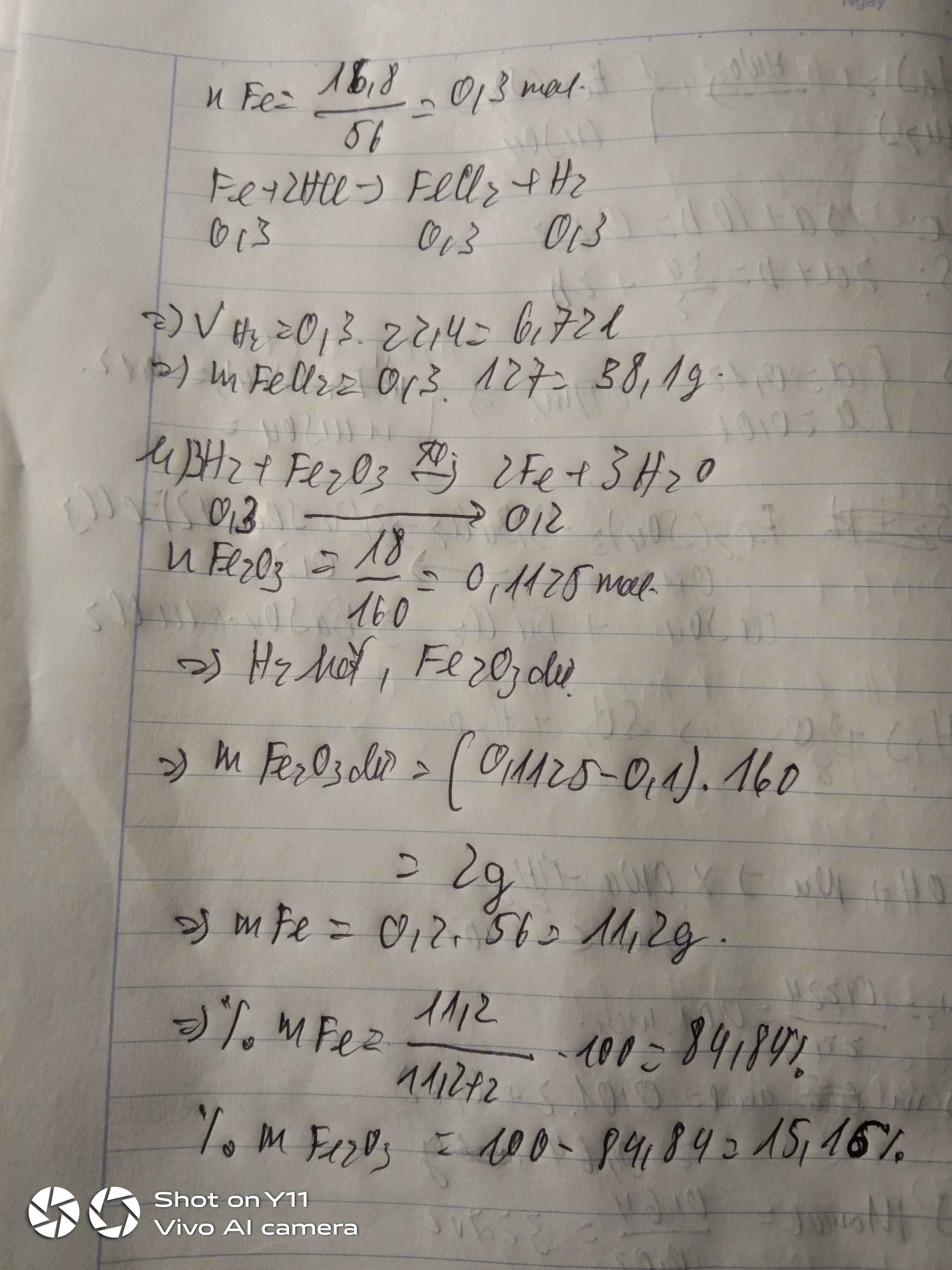
Đáp án: C.
Số mol CH3COOH < Số mol HCOOH.