Một chất hữu cơ Y có thành phần phần trăm theo khối lượng của các nguyên tố như sau: 52,17%C, 13,03%H, phần còn lại là của O. Xác định CTPT của Y, biết tỉ khối hơi của Y so với không khí là 1,59
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(M_A=23.2=46(g/mol)\)
Trong 1 mol A: \(\begin{cases} n_C=\dfrac{46.52,17\%}{12}=2(mol)\\ n_H=\dfrac{46.13,04\%}{1}=6(mol)\\ n_O=\dfrac{46.34,79\%}{16}=1(mol) \end{cases}\)
Vậy \(CTHH_A:C_2H_6O\)

\(Đặt:CTHH:C_xH_yO_z\)
\(x:y:z=\dfrac{52.17}{12}:\dfrac{13.04}{1}:\dfrac{34.78}{16}=4.3475:13.04:2.17375=2:6:1\)
\(CTđơngiản:\left(C_2H_6O\right)_n\)
\(M_Y=\dfrac{9.2}{\dfrac{5.6}{28}}=46\left(\dfrac{g}{mol}\right)\)
\(\Leftrightarrow46n=46\\ \Leftrightarrow n=1\)
\(Vậy:CTHH:C_2H_6O\)

B1 : Tìm khối lượng của mỗi nguyên tố có trong 1 mol hợp chất.
B2 : Tìm số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
B3 : Lập CTHH.

![]()
Ta có
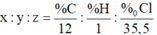
![]()
Do đó công thức phân tử của X có dạng(C2H4Cl)n
Mà ![]()
Vậy chất hữu cơ X là C4H8Cl2
Đáp án A.

a)
-Đặt công thức: NaxSyOz
x=\(\dfrac{32,29.142}{23.100}\approx2\)
y=\(\dfrac{22,54.142}{32.100}\approx1\)
z=\(\dfrac{45,07.142}{16.100}\approx4\)
-CTHH: Na2SO4
Câu b này mình giải cách khác câu a:
nC:nH:nN:nO=\(\dfrac{\%C}{12}:\dfrac{\%H}{1}:\dfrac{\%N}{14}:\dfrac{\%O}{16}=\dfrac{58,5}{12}:\dfrac{4,1}{1}:\dfrac{11,4}{14}:\dfrac{26}{16}\)
nC:nH:nN:nO=4,875:4,1:0,81:1,625=6:5:1:2
-Công thức nguyên: (C6H5NO2)n
-Ta có: (12.6+5+14+16.2)n=123\(\Leftrightarrow\)123n=123\(\Leftrightarrow\)n=1
-CTHH: C6H5NO2

MX = 23.2 = 46(g/mol)
\(m_C=\dfrac{52,17.46}{100}=24\left(g\right)=>n_C=\dfrac{24}{12}=2\left(mol\right)\)
\(m_H=\dfrac{13,05.46}{100}=6\left(g\right)=>n_H=\dfrac{6}{1}=6\left(mol\right)\)
\(m_O=\dfrac{34,78.46}{100}=16\left(g\right)=>n_O=\dfrac{16}{16}=1\left(mol\right)\)
=> CTHH: C2H6O

$\%O = 100\% -52,17\% - 13,03\% = 34,8\%$
$M_Y = 29.1,59 = 46(g/mol)$
CTPT :$C_xH_yO_z$
Ta có :
$\dfrac{12x}{52,17} = \dfrac{y}{13,03} = \dfrac{16z}{34,8} = \dfrac{46}{100}$
Suy ra : x = 2 ; y = 6 ; z = 1
Vậy CTPT là $C_2H_6O$