Cho 15g hỗn hợp Al, Mg đem chia làm 2 phần bằng nhau cho một nửa vài 600ml dung dịch HCl thu được khí A và dung dịch B THU Được 27,9g hỗn hợp muối khan và cho một nửa còn lại vào 800ml dung dịch HCl thu dk 32,5g muối khan
Xác định khối lượng mỗi kim loại trong hỗn hợp
Tính Vh2 dktc ở tn2

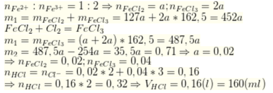
Gọi x,y lần lượt là số mol của Al và Mg trong mỗi phần
=> 27x + 24y =7,5 (1)
Thí nghiệm 1: nHCl (1) ==0,6x => hh muối = 27.9(g)
TN2: nHCl (2) = 0,8x => hh muối = 32.25 g
Ta thấy : nHCl (1)/nHCl (2) < 27,9/32,25
=> Trong TN1 HCl thiếu và trong TN2 HCl dư
Xét TN2
Al + 3HCl --> AlCl3 + 3/2H2
a ----------------> a
Mg + 2HCl --> MgCl2 + H2
b-----------------> b
Từ (1) và (2) => a = 0,1 mol, b= 0,2 mol
=>%m Al = 36%
%mMg =64%
Xét TN1: Vì HCl thiếu nên Mg phản ứng trước, sau đó Al pứ
Vì vậy 27,9 g muối gồm: 0,2 MgCl2 => mMgCl2 = 19g
mAlCl3 = 8,9g
=> nAlCl3 = 1/15 mol
nHCl = 0,4 + 0,2 = 0,6 mol => x=0,1M