bình ga dùng để đun nấu trong gia đình có chứa 13,05 kg (C4H10)ở trạng thái lỏng không được nén dưới áp suất cao. Tính khối lượng không khí cần dùng để đốt hết nhiên liệu có trong bình. Biết O2 chiếm 23% khối lượng của không khí và sản phẩm thu được gồm CO2 và H2O
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đang dạo box Sinh thì thấy bài Hoá:
Đổi 13,05 kg = 13050 g
\(n_{C_4H_{10}}=\dfrac{13050}{58}=225\left(mol\right)\)
PTHH: 2C4H10 + 13O2 \(\underrightarrow{t^o}\) 8CO2 + 10H2O
225 1462,5
=> mO2 = 1462,5 . 32 = 46800 (g)
=> mkk = \(\dfrac{46800}{23\%}=203478,3\left(g\right)\)

nC4H10=\(\frac{13.05}{58}\)= O,225 mol
2C4H10 +13 O2 → 8CO2 + 10H2
0,225 → 1,4625mol
VO2= 1,4625 . 22,4 = 32,76 l
Vì VO2= 20% VKK
suy ra: VKK= 32,76 .5 = 163,8l

Để không khí trong phòng thoáng ta cần có máy hút gió trên bếp hoặc mở cửa trong bếp ăn.

nC4H10=\(\frac{13,05}{58}\)= O,225 mol
2C4H10 +13 O2 → 8CO2 + 10H2
0,225 → 1,4625mol
VO2= 1,4625 . 22,4 = 32,76 l
Vì VO2= 20% VKK
suy ra: VKK= 32,76 .5 = 163,8l

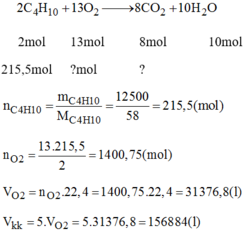
\(n_{C_4H_{10}}=\frac{12500}{58}=215,5\left(mol\right)\)
Phương trình hóa học :
\(2C_4H_{10}+13O_2\rightarrow8CO_2+10H_2O\)
\(2mol\) \(13mol\) \(8mol\)
\(215,5mol\) \(x\) \(mol\rightarrow y\) \(mol\)
a ) \(x=\frac{13\times215,5}{2}=1400,75\left(mol\right)\)
\(V_{kk}=\frac{1400,75\times100\times22,4}{20}=156884\left(lít\right).\)
b ) \(y=\frac{215,5\times8}{2}=862\left(mol\right).\)
\(\rightarrow V_{CO_2}=862\times22,4=19308,8\left(lít\right).\)
Để khong khí trong phòng được thoáng ta cần có máy hút gió trên bếp hoặc mở các của trong bếp ăn .

a: Quá trình 3 sẽ có biến đổi xảy ra
b: Cần: tắt ngay bếp và các nguồn lửa khác xung quanh khu vực đặt bình, đóng ngay van bình gas, cảnh giới cấm lửa tại khu vực bình rò rỉ, thông báo cho các cửa hàng, đại lý hoặc các cơ quan PCCC biết để có biện pháp xử lý
a) Quá trình có xảy ra sự biến đổi hoá học:
(3) Gas bắt lửa và cháy trong không khí chủ yếu tạo thành khí carbon dioxide và nước.

PTHH: 2C4H10 + 13O2 -to> 8CO2 + 10H2O
Ta có:
\(n_{C_4H_{10}}=\frac{13,05}{58}=0,225\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(n_{O_2}=\frac{0,225.13}{2}=1,4625\left(mol\right)\)
Thể tích khí O2 cần dùng (ở đktc):
\(V_{O_2\left(đktc\right)}=1,4625.22,4=32,76\left(l\right)\)
Mà theo giả thiết:
\(V_{O_2}=20\%V_{KK}=\frac{1}{5}V_{KK}\\ < =>V_{KK}=5.V_{O_2}\)
Thể tích không khí cần thiết (ở đktc):
\(V_{KK}=5.V_{O_2}=5.32,76=163,8\left(l\right)\)

Đáp án A
Gọi ![]()
lần lượt là khối lượng ôxi trong bình nước và sau khi dùng:

Mặt khác ![]()
suy ra ![]()
Ghi chú: khi giải bài này ta đã coi khí ôxi ở áp suất 150 atm vẫn là lí tưởng, vì thế kết quả chỉ gần đúng (sai lệch có thể đến cỡ 5%)