bài 1: hòa tan hoàn toàn 8 gam một oxit kim loại R cần vừa đủ dd chứa 10.95 gam HCl.tìm R biết R có hóa trị 3 TRONG HỢP CHẤT TRÊN.
BÀI 2: hòa tan hoàn toàn 5.4 gam một kim loại X trong dd HCl dư thu được 6.72 lít khí (đktc). tìm X.
bài 3: cho 31.2 gam hỗn hợp gồm kim loại Al và Al2O3 tác dụng vừa đủ với dd H2SO4 20% loãng thu được 13.44 lít khí ở đktc.
a. tính tp % theo khối lượng của mỗi chất trong hỗn hợp ban đầu?
b. tính khối lượng dd axit cần dùng.
c. tính C% của mỗi chất có trong dd sau phản ứng.

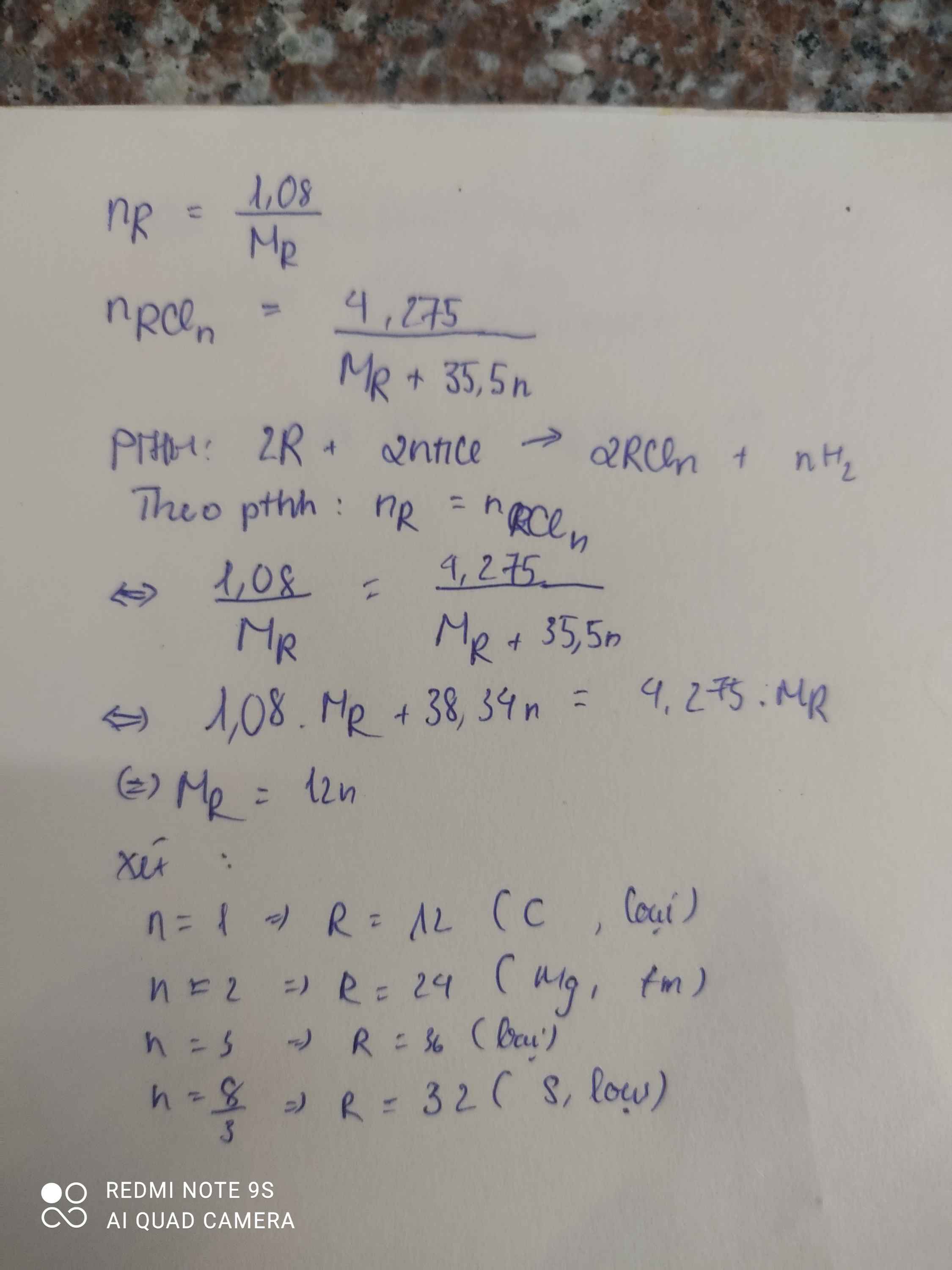
R2O3+6HCl->2RCl3+3H2O
nHCl=0.3(mol)
->nR=0.05(mol)->MR2O3=8:0.05=160(g/mol)
->MR=(160-16*3):2=56(g/mol)->M là Fe
Bài 2
nH2=0.3(mol)
2X+2nHCl->2XCln+nH2(n là hóa trị của kim loại)
nX=0.6:n
+) n=1->MX=9(g/mol)->loại
+)n=2->MX=18(g/mol)->loại
+)n=3->MX=27(g/mol)->X là Al
Bài cuối bạn viết phương trình,chỉ phương trình Al+H2SO4 mới tạo khí thôi,vậy bạn tính được khối lượng nhôm,từ đó tính ra khối lượng nhôm oxit nhé,vì đang vội nên mình không giải giúp bạn được
Bài 3
nH2 = \(\frac{13,44}{22,4}\) = 0,6 mol
2Al + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2 \(\uparrow\) (1)
0,4 <---- 0,6 <-------- 0,2 <------ 0,6 (mol)
Al2O3 + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2O (2)
a) %mAl = \(\frac{0,4.27}{31,2}\) . 100% = 34,62%
%mAl2O3 = 65,38%
b) nAl2O3 = \(\frac{31,2-0,4.27}{102}\) = 0,2 (mol) = nAl2(SO4)3
Theo pt(2) nH2SO4 = 3nAl2O3 = 0,6 (mol)
m dd H2SO4 = \(\frac{\left(0,6+0,6\right)98}{20\%}\) = 588(g)
c) m dd spư = 31,2 + 588 - 0,6 . 2 = 618 (g)
C%(Al2(SO4)3) = \(\frac{\left(0,2+0,2\right)342}{618}\) . 100% = 22,14%