Một oxit của photpho có 43,4% P; 56,6% O. Phân tử khối bằng 142.
Công thức của oxit là:
A: PO B. P2O5 C. P2O D. PO2
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

ta có khối lượng của :
43.4% P = 43.4*100/142= 31
56.6% O= 56.6*100/142 = 40
CTHH của oxit là:
P= 31:31 = 1
O = 40:16 ≃ 3
PO3
Gọi CTHH của oxit là PxOy
Ta có:
x=\(\dfrac{142.43,4\%}{31}=2\)
y=\(\dfrac{142.56,6\%}{16}=5\)
Vậy CTHH của oxit là P2O5

1.
Vì R có hóa trị II \(\rightarrow\) oxit của R là RO
Ta có :\(\%m_{O\left(RO\right)}=19,753\%\rightarrow\%m_R=100\%-19,753\%=80,247\%\)
\(\rightarrow\frac{M_R}{16}=\frac{80,247\%}{19,753\%}\)
\(\rightarrow M_R=65\left(Zn\right)\)
2. Gọi CTHH của oxit sắt là FexOy
\(\rightarrow\frac{56x}{16y}=\frac{7}{3}\rightarrow\frac{x}{y}=\frac{2}{3}\)
Suy ra CTHH là Fe2O3
3. Gọi CTHH cần tìm làm PxOy
\(\%m_O=\frac{31x}{142}=43,4\%\)
\(\rightarrow x=2\rightarrow y=5\)
Vậy CTHH cần tìm là P2O5

-CTHH của oxit đó: \(P_2O_x\).
-Mà oxit đó có phân tử khối là 142 đvC.
\(\Rightarrow31.2+16x=142\)
\(\Leftrightarrow16x=80\)
\(\Leftrightarrow x=5\)
-Vậy công thức hóa học của oxit là P2O5

Đáp án B
Đặt công thức hóa học của oxit là PxOy.
Theo bài ra: 31x + 16y = 142 (1)
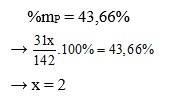
Thay x = 2 vào (1) được y = 5.
Vậy công thức hóa học của oxit là P2O5.

a. Công thức hóa học là : P2O5
b. Công thức hóa học là : Cr2O3

Gọi công thức hóa học của photpho: P x O y
%O = 100 – 43,66 = 5,34%
M P x O y = 31x + 16y = 142
Tỉ lệ khối lượng:
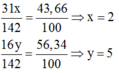
Vậy công thức hóa học của oxit photpho là P 2 O 5 .
Chọn A.

\(n_P=\dfrac{24,8}{31}=0,8mol\)
\(m_O=56,8-24,8=32gam\rightarrow n_O=\dfrac{32}{16}=2mol\)
\(\dfrac{n_P}{n_O}=\dfrac{0,8}{2}=\dfrac{2}{5}\rightarrow P_2O_5\)
Gọi CTHH cần tìm là $P_xO_y$
Ta có :
$\dfrac{31x}{43,4} = \dfrac{16y}{56,6} = \dfrac{142}{100}$
Suy ra : $x = 2 ; y = 5$
Vậy chọn đáp án B
B