Cho dd chứa m gam BaCl2 tác dụng với dd H2SO4 dư tạo thành 4,66gam kết tủa. Tính m.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


H2=0.6 => h2so4 dư. => trong Y có 0.2 mol H2SO4.
Gọi nAl=a, nFeSO4=b. Ta có: 3a+2b=1.2 và 27a+56b=22.2
=>a=0.2, b=0.3
Dd y: fe2+: 0.3, al3+: 0.2, so4 2-: 0.8 và h- 0.4
Y td vs ba(oh)2 dư
=> kt thu đc là fe(oh)2: 0.3 mol bà baso4 0.8 mol
*lưu ý al3+ k tạo kt vì oh- dư
=> m kt=213.4g
H2=0.6 => h2so4 dư. => trong Y có 0.2 mol H2SO4.
Gọi nAl=a, nFeSO4=b. Ta có: 3a+2b=1.2 và 27a+56b=22.2
=>a=0.2, b=0.3
Dd y: fe2+: 0.3, al3+: 0.2, so4 2-: 0.8 và h- 0.4
Y td vs ba(oh)2 dư
=> kt thu đc là fe(oh)2: 0.3 mol bà baso4 0.8 mol
*lưu ý al3+ k tạo kt vì oh- dư
=> m kt=213.4g

6NaOH + Al2(SO4)3 -> 2Al(OH)3 + 3Na2SO4 (1)
CT: NaOH + Al(OH)3 -> NaAlO2 + 2H2O (2)
nAl2(SO4)3=0,1(mol)
nAl(OH)3=0,1(mol)
Xét TH1: Al2(SO4)3 dư
Từ 1:
nNaOH=3nAl(OH)3=0,3(mol)
CM dd NaOH=\(\dfrac{0,3}{0,25}=1,2M\)
Xét TH2: NaOH dư
Từ 1:
nAl(OH)3 ở (1)=2nAl2(SO4)3=0,2(mol)
nNaOH ở (1)=6nAl2(SO4)3=0,6(mol)
Từ 2:
nNaOH ở (2)=nAl(OH)3=0,1(mol)
CM dd NaOH=\(\dfrac{0,7}{0,25}=2,8M\)

Phương trình: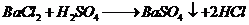
Vậy kết tủa là
Số mol
Phương trình
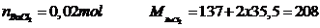

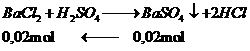
Vậy m là