Bài 1:
Nung 10,2 g hỗn hợp Al, Mg, Na trong khi O2 dư. Sau phản ứng kết thúc thu dc 17g hỗn hợp chất rắn. Mặt khác cho hỗn hợp trên td với HCl dư thấy thoát ra V lít khí và dung dịch A. Cô cạn dung dich A thì thu dc m gam muối clorua khan. Tinh V và m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi số mol Al, Mg, Na là a, b,c (mol)
- Xét TN1:
\(n_{O_2}=\dfrac{17-10,2}{32}=0,2125\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
a-->0,75a
2Mg + O2 --to--> 2MgO
b--->0,5b
4Na + O2 --to--> 2Na2O
c--->0,25c
=> 0,75a + 0,5b + 0,25c = 0,2125
- Xét TN2:
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
a------------->a----->1,5a
Mg + 2HCl --> MgCl2 + H2
b------------->b------>b
2Na + 2HCl --> 2NaCl + H2
c-------------->c---->0,5c
nH2 = 1,5a + b + 0,5c = 0,2125.2 = 0,425 (mol)
=> V = 0,425.22,4 = 9,52 (l)
Có: \(n_{HCl}=2.n_{H_2}=0,425.2=0,85\left(mol\right)\)
Theo ĐLBTKL: mkim loại + mHCl = mmuối + mH2
=> 10,2 + 0,85.36,5 = m + 0,425.2
=> m = 40,375 (g)

a)
$4Na + O_2 \xrightarrow{t^o} 2Na_2O$
$2Mg + O_2 \xrightarrow{t^o} 2MgO$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
$2Na + 2HCl \to 2NaCl + H_2$
$Mg + 2HCl \to MgCl_2 + H_2$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
b)
Bảo toàn khối lượng : $m_{O_2} = 4,08 - 2,48 = 1,6(gam)$
$n_{O_2} = \dfrac{1,6}{32} = 0,05(mol)$
Đốt 2,48 gam X cần 0,05 mol $O_2$
Suy ra, đốt 4,96 gam X cần 0,1 mol $O_2$
Mà : \(\dfrac{1}{4}n_{Na}+\dfrac{1}{2}n_{Mg}+\dfrac{3}{4}n_{Al}=n_{O_2}=0,1\)
Theo PTHH :
\(n_{H_2}=\dfrac{1}{2}n_{Na}+n_{Mg}+\dfrac{3}{2}n_{Al}=2\left(\dfrac{1}{4}n_{Na}+\dfrac{1}{2}n_{Mg}+\dfrac{3}{4}n_{Al}\right)=2.0,1=0,2\)$V = 0,2.22,4 = 4,48(lít)$
$n_{HCl} = 2n_{H_2} = 0,4(mol)$
Bảo toàn khối lượng : $m = 4,96 + 0,4.36,5 - 0,2.2 = 19,16(gam)$

Coi hỗn hợp kim loại trên là R có hóa trị n
\(4R + nO_2 \xrightarrow{t^o} 2R_2O_n\\ m_{O_2} = 17-10,2 = 6,8(gam) \Rightarrow n_{O_2} = \dfrac{6,8}{32} = 0,2125(mol)\\ n_R = \dfrac{4}{n}n_{O_2} = \dfrac{0,85}{n}(mol)\\ 2R + 2nHCl \to 2RCl_n + nH_2\\ n_{H_2} = \dfrac{n}{2}n_R = 0,425(mol)\\ \Rightarrow V = 0,425.22,4 = 9,52(lít)\\ n_{HCl} = 2n_{H_2} = 0,85(mol)\\ \text{Bảo toàn khối lượng : }\\ m_{muối} = m_{kim\ loại} + m_{HCl} - m_{H_2} = 10,2 + 0,85.36,5 - 0,425.2 = 40,375(gam)\)

\(BTKL:\)
\(m_{O_2}=34-20.4=13.6\left(g\right)\)
\(n_{O_2}=\dfrac{13.6}{32}=0.425\left(mol\right)\)
\(BTNTO:\)
\(n_{H_2O}=2n_{O_2}=2\cdot0.425=0.85\left(mol\right)\)
\(BTNTH:\)
\(n_{HCl}=2n_{H_2O}=2\cdot0.85=1.7\left(mol\right)\)
\(m_{Muối}=m_{Kl}+m_{Cl^-}=20.4+1.7\cdot35.5=80.75\left(g\right)\)

1)
mHCl = 25,55.100/100=25,55(g)
=> nHCl = 25,55/36,5=0,7(mol)
Pt: Mg + 2HCl --> MgCl2 + H2
Zn + 2HCl --> ZnCl2 + H2
2Al + 6HCl --> 2AlCl3 + 3H2
+Giả sử trong hh chỉ có Mg
nMg = 5,624=0,235,624=0,23 mol
Pt: Mg +......2HCl
0,23 mol-> 0,46 mol < 0,7 (mol)
=> HCl dư
<=> Hh Mg, Zn, Al bị hòa tan hết

4Al+3O2--->2Al2O3
2Mg+O2--->2MgO
4Na+O2--->2Na2O
mO2=m chất rắn-mhh=17-10,2=6,8(g)
=>nO2=6,8/32=0,2125(mol)
2Al+6HCl--->2AlCl3+3H2
Mg+2HCl--->MgCl2+H2
2Na+2HCl--->2NaCl+H2
Theo pt: nH2=2nO2=2.0,2125=0,425(mol)
=>VH2=0,425.22,4=9,52(l)
Theo pt: nHCl=2nH2=2.0,425=0,85(mol)
=>nCl-=0,85(mol)
=>mCl-=0,85.35,5=30,175(g)
m muối=m kim loại +mCl-=10,2+30,175=40,375(g)

\(n_{H_2}=\dfrac{0,336}{22,4}=0,015mol\)
\(\Rightarrow n_{HCl}=2n_{H_2}=2\cdot0,015=0,03mol\)
\(\Rightarrow n_{Cl^-}=0,03mol\Rightarrow m_{Cl^-}=1,065g\)
\(m_{CRắn}=m_{kl}+m_{Cl^-}=1,065+1,5=2,565g\)
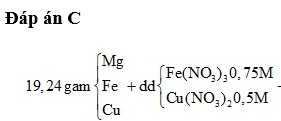
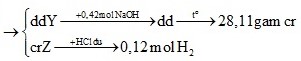


4R+nO2 ------->2R2On
0,85/n <---0,2125
2R+ 2nHCl ------->2RCln+nH2
0,85/n --->0,85 0,425
Ta có nO2 p/ư =(17-10,2):32=0,2125 mol
VH2=0,425.22,4=9,52 l
m muối =10,2+0,85.36,5-0,425.2=40,375 g