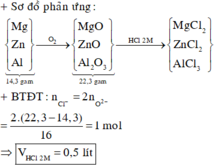
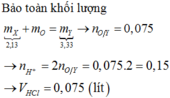Cho 2.13 gam hỗn hợp X gồm Mg, Cu và Al ở dạng bột tác dụng hoàn toàn với oxi thu được hỗn hợp Y gồm các oxit có khối lượng 3.33 gam. Tính thể tích dung dịch HCl 2M vừa đủ để phản ứng với Y.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Chọn đáp án C
n H C l = 2 n O o x i t = 2 3 , 33 - 2 , 13 16 = 0,15 (mol)
→ V d d H C l = 0 , 15 0 , 2 = 0,075 (lít)

tham khảo
Bảo toàn khối lượng:
m kim loại+ mO2= moxit
=> mO2= 3.33-2.13=1.2g
=> nO2= 1.2/32=0.0375mol
=>nO=0.075mol
mà cứ 1O + 2H+ = 1H2O
=> 0.075mol 0.15mol
vậy nH+ cần dùng là 0.15mol
mà CM=n / V => V= n / CM = 0.15 / 2 = 0.075l =75ml

mtăng=mO=3,33-2,13=1,2g
nO=1,2 : 16= 0,075 mol
nH2SO4 = nO(trong oxit)=0,075mol
VddHCl =0,075:2=0,0375 lit=37,5 ml

nH2SO4=2.0,2=0,4mol
PTHH: 2NaOH+H2SO4=> Na2SO4+2H2O
0,8mol<-0,4mol->0,4mol->0,8mol
theo định luật btoan khói lượng mdd Na2SO4
= mNaOH+mH2SO4-mH2O=0,8.40+1,3.0,4.-0,8.18=56,6g
mNa2SO4=04.142=56,8
=> C%=32,25%
Bài 1: PTHH: 2NaOH + H2SO4 --> Na2SO4 + 2H2O
Đổi: 200 ml = 0,2 lít
Số mol của H2SO4 là: 0,2 . 2 = 0,4 mol
Khối lượng dung dịch axit là: 200 . 1,3 = 260 gam
Khối lượng của NaOH là: 0,4 . 2 . 40 = 32 gam
Khối lượng dung dịch sau phản ứng là: 260 + 32 = 292 gam
Khối lượng Na2SO4 là: 0,4 . 142 = 56,8 gam
Nồng độ phần trăm Na2SO4 có trong dung dịch sau phản ứng là: ( 56,8 : 292 ) . 100% = 19,5%

Ta có mO = 3.33 - 2.13 = 1.2g -> nO = 0.075mol
Ta có: 2H+ + O-2 -> H2O
------- 0.15 <-0.075
-> V HCl = 0.15 : 0,6 = 250 ml
-> Đáp án D