hòa tan hoàn toàn 3.6 gam kim loại Mg cần phải dùng bao nhiêu ml dung dịch hỗn hợp HCl 1M và H2SO4 0.75M?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_O=\dfrac{33,3-21,3}{16}=0,75\left(mol\right)\)
=> nH2O = 0,75 (mol)
Giả sử có V lít dd
=> \(\left\{{}\begin{matrix}n_{H_2SO_4}=V\left(mol\right)\\n_{HCl}=2V\left(mol\right)\end{matrix}\right.\)
Bảo toàn H: 2V + 2V = 0,75.2
=> V = 0,375 (lít) = 375 (ml)

Giải thích: Đáp án C
nHCl = 0,8.1 = 0,8 (mol) ; nH2SO4 = 0,8 (mol)
Vì phản ứng vừa đủ => mmuối = mKL + mCl- + mSO42- = 39,8 + 0,8.35,5 + 0,8.96 = 145 (g)

Cho thể tích của dung dịch là V (l)
\(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=0,5V\left(mol\right)\\n_{H_2SO_4}=V\left(mol\right)\end{matrix}\right.\)
PTHH:
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(0,25V\leftarrow0,5V\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(V\leftarrow V\)
Ta có: \(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
\(\Rightarrow V+0,25V=0,1\Rightarrow V=\dfrac{0,1}{1,25}=0,08\left(l\right)=80\left(ml\right)\)
Vậy: ...

Đáp án A
M + H2SO4 → MSO4 + H2 (1)
2KOH + H2SO4 → K2SO4 + 2H2O (2)
![]()
Mà
![]()
![]()
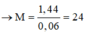
M là Magie

PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
a_____3a_______a______\(\dfrac{3}{2}\)a (mol)
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
b_____2b_______b_____b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}27a+24b=2,055\\3a+2b=0,205\cdot1\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,045\\b=0,035\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{AlCl_3}=0,045\cdot133,5=6,0075\left(g\right)\\m_{MgCl_2}=0,035\cdot95=3,325\left(g\right)\end{matrix}\right.\)


. nMg = 3,6/24= 0,15 (mol)
Gọi x là V dd A --> n HCl = x mol
n H2SO4 = 0,75x mol
Mg + 2HCl ---> MgCl2 + H2
1mol 2mol
x/2 <--x
Mg + H2SO4 ---> MgSO4 + H2
1mol 1mol
0,75x <--0,75x
n Mg = x/2 + 0,75x = 0,15 (mol)
x + 1,5x = 0,3
x = 0,12 (l)