1) Phải đốt bao nhiêu gam cacbon để khi cho khí CO2 tạo ra trong pứ trên tác dụng với 3,4 lít dd NAOH 0,5M ta đc 2 muối với nồng độ mol muối hidrocacbonat bằng 1,4 lần nồng độ mol của muối trung hòa?
2) Nếu thêm một lượng vừa đủ dd CaCl2 1M thì sẽ đc bao nhiêu gam kết tủa? Tính thể tích dd CaCl2 phải dùng

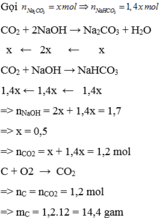
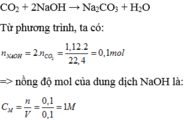
1) CO2+NaOH-->NaHCO3
CO2+2NaOH-->Na2CO3+H2O
nNaOH=1,7mol
tỉ lệ nồng độ mol=tỉ lệ số mol
-->1,4nNaHCO3=nNa2CO3
gọi nNa2CO3=x--->nNaHCO3=1,4x
-->nNaOH(1)=1,4x, nNaOH(2)=2x
hay 1,7=1,4x+2x
-->x=0,5
-->tổng số mol CO2=1,2mol
-->mC=1,2.12=14,4g
2) Khi thêm lượng vừa đủ dung dịch CaCl2 vào dung dịch chứa 2 muối trên chỉ xảy ra p/ư:
CaCl2 + Na2CO3 ---> CaCO3 (rắn)+ 2NaCl (3)
Từ p/ư (3): số mol CaCl2 = số mol Na2CO3 = số mol CaCO3 = 3,4x 5/34 = 0,5 (mol)
=> Khối lượng kết tủa CaCO3 = 0,5 . 100 = 50 (g)
=> Thể tích dung dịch CaCl2 phải dùng: 0,5 : 1 = 0,5 lít.
cho tui hỏi xíu vì sao co2 +naoh->2nahco3