Nêu cách pha chế 604g dung dịch KCl bão hòa ở 80oC từ KCl và nước. Biết SKCl(80oC) = 51g
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) m KCl = 300.5% = 15(gam)
m dd KCl = 15/15% = 100(gam)
m nước cần thêm = 300 - 100 = 200(gam)
Pha chế :
- Chuẩn bị 100 gam dung dịch KCl 15% vào cốc 1 lít
- Đong thêm 200 gam nước vào cốc,khuấy đều
b) n BaCl2 = 0,2.1 = 0,2(mol)
V dd BaCl2 2M = 0,2/2 = 0,1(lít) = 100(ml)
V nước cần thêm = 200 - 100 = 100(ml)
Pha chế :
- Chuẩn bị 100 ml dd BaCl2 2M vào cốc 500 ml
- Đong thêm 100 ml nước vào cốc,khuấy đều

2
160 gam dung dịch CuSO4 chứa mCuSO4=160.10%=16 gam
-> nCuSO4=16/160=0,1 mol
-> mH2O=160-16=144 gam -> nH2O\(=\dfrac{144}{18}\)=8 mol
-> số mol các nguyên tử trong dung dịch=8.3+0,1.6=24,6 mol
-> Sau khi cô cạn số mol các chất =\(\dfrac{24,6}{2}\)=12,3 gam
-> nH2O thoát ra =\(\dfrac{12,3}{3}\)=4,1 mol -> mH2O=4,1.18=73,8 gam

Câu 2:
1.
\(m_{H_2O}=\dfrac{600}{100+50}.100=400\left(g\right)\\ m_{CuSO_4\left(kết.tinh\right)}=\dfrac{400}{100}.\left(50-15\right)=140\left(g\right)\\ n_{CuSO_4.5H_2O}=n_{CuSO_4}=\dfrac{140}{160}=0,875\left(mol\right)\\ m_{CuSO_4.5H_2O\left(kết.tinh\right)}=0,875.250=218,75\left(g\right)\)
2,
Số nguyên tử bằng một nửa ban đầu => số mol giảm đi một nửa
\(m_{CuSO_4}=160.10\%=16\left(g\right)\Rightarrow n_{CuSO_4}=\dfrac{16}{160}=0,1\left(mol\right)\\ m_{H_2O}=160-16=144\left(g\right)\Rightarrow n_{H_2O}=\dfrac{144}{18}=8\left(mol\right)\\ \Rightarrow n_{H_2O\left(bay.hơi\right)}=\dfrac{1}{2}.\left(0,1+8\right)=4,05\left(mol\right)\\ \Rightarrow m_{H_2O\left(bay.hơi\right)}=4,05.18=72,9\left(g\right)\)

\(\dfrac{S}{S+100}=\dfrac{m_{ct}}{m_{bãohòa}}\Rightarrow\dfrac{35,9}{35,9+100}=\dfrac{m_{ct}}{5\cdot1000}\)
\(\Rightarrow m_{ct}=1320,824g=1,32kg\)

Chọn B
Độ tan của R 2 S O 4 ở 80 o C là 28,3 gam
→ Trong 1026,4 gam dung dịch có
m R 2 S O 4 = 1026,4.28,3 100 + 28,3 = 226,4 g

Vậy kim loại R là Na.

Ở 20 0 C thì 75g nước hòa tan tối đa muối NaCl có khối lượng:
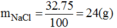
Vậy dung dịch NaCl đã pha chế là chưa bão hòa. Để dung dịch NaCl bão hòa ở nhiệt độ này, ta cần cho thêm vào dung dịch đã pha chế một lượng NaCl là: 24-23,5=0,5(g)

*Ở 90oc
Cứ 100g nước thì hòa tan tối đa được 51g KCl để tạo thành 151g ddKCl bão hòa
Cứ x(g)nước thì hòa tan tối đa được y(g)KCl để tạo thành 604g dd KCl bão hòa
⇒mH2O/90o = x = \(\dfrac{604.100}{151}=400\) (g)
⇒mKCl/90o = y = mdd - mH2O = 604-400=204 (g)
ta có :
mH2O/10o = mH2O/90o = 400 (g)
*Ở 10oc :
Cứ 100g nước hòa tan tối đa 34 g KCl
Vậy 400g nước hòa tan tối đa z (g) KCl
⇒mKCl/10o = z =\(\dfrac{400.34}{100}136\) (g)
⇒mKCl/kt = mKCl/90o - mKCl/10o =204 -136 = 68 (g)
Vậy khối lượng của KCl kết tinh là : 68 g

a) \(n_{KCl}=0,3.2=0,6\left(mol\right)\)
=> \(m_{KCl}=0,6.74,5=44,7\left(g\right)\)
b) \(m_{NaOH}=20.25\%=5\left(g\right)\)
c) \(S=\dfrac{m_{ct}}{m_{dd}}.100\)
=> \(53,6=\dfrac{m_{MgCl_2}}{100}.100\)
=> mMgCl2 = 53,6 (g)