Cho 25g nước clo vào một dd có chứa 2,5g KBr thấy dd chuyển sang màu vàng và KBr vẫn dư. Cô cạn dd sau phản ứng thu được 1,61g chất rắn khan. Giả sử toàn bộ clo trong nước clo đã phản ứng hết. Hãy tính nồng độ % của clo trong nước clo ban đầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi số mol Cl2 là a (mol)
PTHH: 2KBr + Cl2 --> 2KCl + Br2
2a<----a------->2a
=> mrắn sau pư = 2,5 - 119.2a + 74,5.2a = 1,61
=> a = 0,01 (mol)
\(C\%_{Cl_2}=\dfrac{0,01.71}{25}.100\%=2,84\%\)
Rắn thu được gồm \(\left\{{}\begin{matrix}KBr\\KCl\end{matrix}\right.\)
mKBr = 2,5 - 0,02.119 = 0,12 (g)
mKCl = 0,02.74,5 = 1,49 (g)

Bài 15. Lời giải:
16HCl + 2KMnO4 → 2KCl + 2MnCl2 + 8H2O + 5Cl2
Theo PTHH : \(n_{KCl}=n_{MnCl_2}=x\)
Khối lượng muối = 28,07 ⇒ \(m_{KCl}+m_{MnCl_2}=28,7\)
⇒ x . 74,5 + x . 126 = 28,07
⇒ x = 0,14 mol
\(\Rightarrow n_{KCl}=n_{MnCl_2}=0,14mol\)
Theo PTHH ⇒ \(n_{Cl_2}=\frac{5}{2}n_{KCl}=\frac{5}{2}.0,14=0,35mol\)
Theo định luật bảo toàn e : \(x.n_M+3n_{Al}=2n_{Cl_2}=0,7mol\)
Có tỉ lệ mol Al : M = 1 : 2 \(\Rightarrow\) nAl = a thì nM = 2a
⇒ 2a.x + a.3 = 0,7 mol
Với x = 1 ⇒ a = 0,175 mol ⇒ m Al = 0,175.27 = 4,725 gam
⇒ mM = 7,5 – 4,725 = 2,775 gam
⇒ \(M_M=\frac{2,775}{0,175.2}=7,9\)(loại)
Với x = 2 ⇒ a = 0,1 mol ⇒ mAl = 27.0,1 = 2,7 gam ⇒ m M = 7,5 – 2,7 = 4,8 gam
\(\Rightarrow M_M=\frac{4,8}{0,1.2}=24\)(Mg, chọn)
Vậy kim loại cần tìm là Mg
Bài 14. Lời giải:
\(Cl_2+2NaBr\rightarrow2NaCl+Br_2\\ n_{Cl_2}=\frac{2,5-1,61}{44,5}=0,02\left(mol\right)\\ C\%_{Cl_2}=\frac{0,02.71}{25}.100\%=5,68\%\)

Gọi số mol clo đã phản ứng là x (mol)
PTHH : Cl2 + 2KBr \(\rightarrow\) 2KCl + Br2
x 2x 2x x (mol)
\(\Rightarrow m_{KBr_{dư}}=3,125-2x.\left(80+39\right)=3,125-238x\left(g\right)\)
mrắn khan = \(m_{KBr_{dư}}\)+ mKCl
\(\Leftrightarrow2,0125=3,125-238x+2x.74,5\)\(\Leftrightarrow\) x = 0,0125 (mol)
\(\Rightarrow m_{Cl_2}=0,0125.71=0,8875\left(g\right)\)
\(C\%_{Cl_2}=\dfrac{0,8875}{31,25}.100\%=2,84\%\)

Khi cho 5g Br 2 có lẫn Cl 2 phản ứng với KBr thì khối lượng muối giảm là :
1,600 - 1,155 = 0,445 (g)
Cl 2 + 2KBr → 2KCl + Br 2
Lý thuyết: 71 g 238 g 149 g khối lượng muối giảm đi 238 – 149 = 89 g
Thực tế: x g 0,445 g khối lượng muối giảm
Ta có:
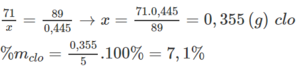

4)
3Cl2 + 6KOH = 5KCl + KClO3 + 3H2O
0,3 0,6 0,5
ta có nCl2 = 0,6 mol
mà nKCl sinh ra = 0,5 mol => Cl2 dư
nKOH = 6/5nKCl = 0,6 mol => CMKOH = 0,6/2,5 = 0,24 M
NaX+AgNO\(_3\)\(\rightarrow\)AgX\(\downarrow\)+NaNO\(_3\)
0,01 0,01 (mol)
2AgX\(\rightarrow\)2Ag+X\(_2\)
0,01 0,01 (mol)
n\(_{Ag}\)=\(\dfrac{1,08}{108}\)=0,01(mol)
M\(_{NaX}\)=\(\dfrac{1,03}{0,01}\)=103(g)
→M\(_X\)=103-23=80(g)
vậy X là Brom(Br)

\(n_{Fe}=\dfrac{14}{56}=0,25\left(mol\right)\\ n_{Cl_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ 2Fe+3Cl_2\rightarrow\left(t^o\right)2FeCl_3\\ Vì:\dfrac{0,3}{3}< \dfrac{0,25}{2}\Rightarrow Fedư\\ n_{FeCl_3}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\\ m_{FeCl_3}=162,5.0,2=32,5\left(g\right)\\ \Rightarrow D\)
\(Cl_2+2NaBr\rightarrow2NaCl+Br_2\)
\(n_{Cl_2}=\frac{2,5-1,61}{44,5}=0,02\left(mol\right)\)
\(C\%_{Cl_2}=\frac{0,02.71}{25}.100\%=5,68\%\)
Cl2+2NaBr→2NaCl+Br2
nCl2=2,5−1,6144,5=0,02(mol)
C%Cl2=0,02.7125.100%=5,68%